4 Antociani, piranoantociani in barva vina
Jelena Topić Božič
Center za krožno gospodarstvo, Rudolfovo – Znanstveno in tehnološko središče, Novo mesto, Slovenija
Fakulteta za industrijski inženiring Novo mesto, Novo mesto, Slovenija
jelena.topic.bozic@rudolfovo.eu
Uvod
Fenolne spojine so spojine, ki prispevajo k organoleptičnim lastnostim vina, zlasti barvi, trpkosti in grenkobi. Kemijsko imajo fenolne spojine vsaj en fenolni obroč z vsaj eno hidroksilno skupino (Waterhouse in sod., 2016). V enološko kemijski literaturi za to skupino sekundarnih metabolitov najdemo tudi izraze, kot so polifenoli, biofenoli.
Fenolne spojine v vinu lahko razdelimo v dve skupini: neflavonoidne in flavonoidne fenolne spojine (He in sod., 2012a). Flavonoidi so najpogostejše fenolne spojine v grozdju in vinih. Družina flavonoidov se nadalje deli na podskupine flavonov, flavanolov, flavanonov in antocianov. Neflavonoidne fenole pa delimo na fenolne alkohole, fenolne kisline, hidroksicimetne kisline in stilbene (Waterhouse in sod., 2016).
Po Macheixu (1990) antociani vključujejo antocianidine in glikozilirane derivate antocianidinov – antocianine. Antocianidini so v naravi le redko prisotni in nastajajo v vzorcih največkrat zaradi priprav bioloških vzorcev za analizo. Brez glikozilacije so namreč zelo nestabilni in kmalu razpadejo (Macheix, 1990).
Naravno prisotni antociani so torej glikozilirani derivati aglikonskih delov antocianidinov. Najbolj pogoste antocianidine med njimi poznamo pod imenom delfinidin, petunidin, cianidin, peonidin in malvidin. Med sabo se razlikujejo po barvi katero odraža stopnja hidroksilacije in metoksilacije obroča B – mesti R1 in R2 na fenolnem obroču (Slika 1). Nadaljnja raznolikost antocianov iz vina/grozdja je posledica acilacije glikozidno vezane glukoze s hidroksicimetnimi kislinami (kavna kislina, p-kumarna kislina) ali alifatskimi kislinami, kot je ocetna kislina (He in sod., 2010; Lorrain in sod., 2013; Panche in sod., 2016; Waterhouse in sod., 2016). Antociani so naravni pigmenti, odgovorni za rdečo, modro in vijolično barvo sadja, zelenjave, rož in zelišč. Njihovo ime izhaja iz grškega anthos, kar pomeni roža, in kyanos, kar pomeni modro (Welch in sod., 2008).
Rdeča barva vin in grozdja izvira iz antocianov, ki so značilni predvsem za rdeče sorte grozdja. Večinoma se nahajajo v jagodni kožici, razen pri nekaterih sortah grozdja z obarvanim mesom. V pridelavi rdečih vin se po drozganju in med maceracijo izločajo v mošt in vino. S časom maceracije se izplen antocianov povečuje, vendar je odvisen tudi od fenolne zrelosti grozdja. Grozdje sort Vitis vinifera L. vsebuje večinoma monomerne antociane, kot so -3-O-monoglikozidi delfinidina, cianidina, petunidina, peonidina in malvidina. Najbolj zastopan antocian v rdečem vinu sort Viris vinifera L. je malvidin-3-O-glukozid, ki ima na mestu R1 in R2 metoksi skupino (sledi -3-O-glukozid peonidina, ki imata eno prosto skupino -OH na B-obroču (Freitas in sod., 2017; He in sod., 2010; Lorrain in sod., 2013) (Tabela 1). Pri sortah, ki niso Vitis vinifera L., pa se glikozilacija zgodi na mestih 3 in 5 (Sabra in sod., 2021).
Celokupna koncentracija antocianov v vinih je sortno pogojena. Waterhouse (2002) je ocenil, da je koncentracija v mladih vinih največkrat okoli 500 mg/L, v staranih vinih pa 90 mg/L (Waterhouse, 2002). V nekaterih primerih lahko skupna koncentracija preseže 2000 mg/L. Med različnimi sortami se koncentracije antocianov lahko zelo razlikujejo (Nikfardjam in sod., 2006). Nikfardjam in sod. (2006) so izvedli raziskavo, v kateri so ugotovili, da je povprečna koncentracija monomernih antocianov 831 mg/L v vinu sorte cabernet franc, medtem ko je bila koncentracija v pinot noir vinu 447 mg/L. Povprečna koncentracija v portovcih je bila 1642 mg/L (Nikfardjam in sod., 2006). Koncentracije posameznih antocianov zelo variirajo, v večini vin pa je večinoma prisoten malvidin-3-O-glikozid kot glavni prosti antocian (Lorrain in sod., 2013). Osnovna struktura glikoziliranih antocianov je prikazana na Sliki 1. Sladkorji so vezani preko glikozidne vezi na mestu C-3, diglikozidi pa tudi na mestu C-5 antocianidina. V grozdju in vinu so glikozilirani z glukozo. Antocianini so razširjeni v rdečem in modrem sadju ter zelenjavi, njihova vsebnost v rastlinah pa je med vrstami zelo različna. Poleg glikozilacije z glukozo se pojavljajo še drugi sladkorji, med njimi galaktoza, ramnoza, arabinoza in ksiloza (Merecz-Sadowska in sod., 2023).
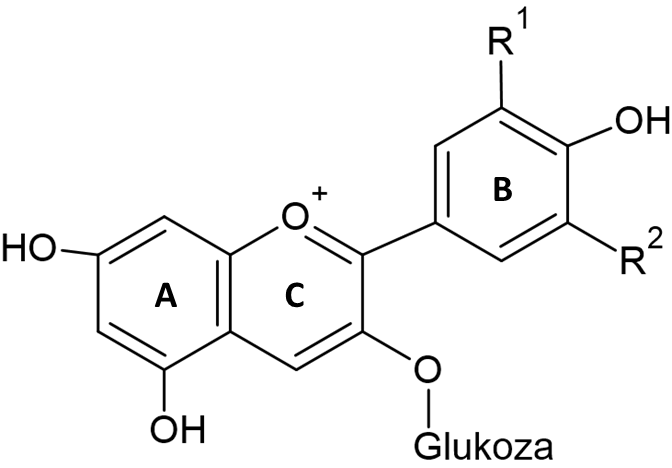
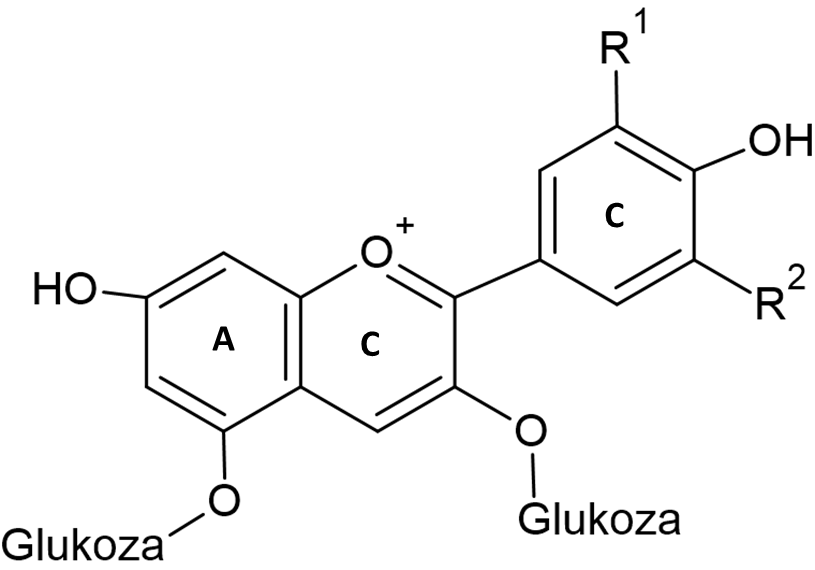
Med seboj se razlikujejo glede na to, kateri skupini sta vezani na obroč B (Tabela 1) na mestih R1 in R2 (Slika 1). Njihov izplen pri pridelavi vina je odvisen od sorte grozdja, zrelosti, sezonskih razmer, vinogradniških praks, lege vinogradov in samih tehnoloških parametrov pridelave vina. Koncentracija antocianov v vinu je namreč odvisna tudi od pogojev fermentacije, kot so temperatura med fermentacijo ter čas in temperatura maceracije. Prisotnost skupnih antocianov in posameznih antocianov pa se v vinih spreminja tudi med staranjem vina (Champ and Kundu-Champ, 2019; He in sod., 2012a; Minnaar in sod., 2018).
Tabela 1. Kemijske strukture najpogostejših antocianov v rdečem grozdju in vinu (R1 in R2 v povezavi s Sliko 1).
|
Antocianin |
Struktura R1 |
Struktura R2 |
|
delfinidin-3-O-glikozid |
OH |
OH |
|
cianidin-3-O-glikozid |
OH |
H |
|
petunidin-3-O-glikozid |
OH |
OCH3 |
|
peonidin-3-O-glikozid |
OCH3 |
H |
|
malvidin-3-O-glikozid |
OCH3 |
OCH3 |
Antociani se pri mletju in drozganju že izločajo v grozdni sok ter že takrat začnejo reagirati z drugimi spojinami vina, kot so drugi fenoli, pa tudi polimerne spojine, kot so polisaharidi, ki pomagajo zaščititi monomerne antociane pred razbarvanjem zaradi kislega pH-ja mošta, ki se ponavadi giblje v območju 3,1 – 3,6 (Boulton in sod., 1996; Moreno in Peinado, 2012).
To lahko opazimo s spremembo barve iz začetne modrovijolične barve v temno rdečo barvo, kar imenujemo kopigmentacija. Gre za pomemben pojav v pridelavi rdečih vin, saj vpliva na barvno stabilnost in intenzivnost vina v različnih življenjskih obdobjih. Kopigmentacija je kemijska interakcija med antocianini, naravnimi pigmenti v grozdnih jagodah in brezbarvnimi fenolnimi spojinami, kot so flavonoli ali hidroksicimetne kisline, ter drugimi spojinami vina. Kopigmentacija izboljša barvo vina, tako da poveča absorpcijo svetlobe (hiperkromni učinek) in premakne barvni odtenek v modrordeče tone (batohroni premik). Ta interakcija ohranja intenzivno barvo v zgodnjih fazah staranja vina, ko so antociani še v velikih koncentracijah (Boulton in sod., 1996; Moreno and Peinado, 2012). Kopigmentacija tako omogoča pridelovalcem rdečih vin izboljšanje vizualne kakovosti vina, povečuje njegovo stabilnost in podaljšuje trajnost barvne intenzitete, kar je ključno za tržno privlačnost vina.
Reakcije antocianov z drugimi spojinami se nadaljujejo tudi pri fermentaciji in maceraciji, ko začnejo reagirati z drugimi produkti fermentacije in grozdja ter fenolnimi spojinami. Poznavanje teh sprememb lahko pomaga vinarju izboljšati kakovost vina oz. spremembe v vinu glede na čas. Te spremembe so še posebej vidne v rahleje obarvanih rdečih ali rosé vinih, pri katerih barvne note prehajajo iz lepe rdeče ali rožnate barve (pri roséjih) v opečnate tone.
Tudi med zorjenjem in staranjem vina antociani nadalje reagirajo z drugimi spojinami v vinu, kar povzroči nastanek novih pigmentov. Imenujemo jih piranoantociani. Med njimi so najbolj poznani vitizini in vinilfenolni piranoantociani. Zaradi prisotnosti teh spojin se spreminja barva vina med staranjem (Alcalde-Eon in sod., 2006; He in sod., 2012b), saj je zanje značilna večja intenzivnost barve, poleg tega so stabilnejše v kemijskem okolju vina (če vino razumemo kot raztopino). Manj so dovzetne za spremembe v vrednosti pH in koncentraciji kisika, odpornejše pa so na razbarvanje z žveplovim dioksidom in temperaturo (Freitas in sod., 2017). Zato so te spojine zanimive tudi kot možna naravna barvila v drugih živilskih izdelkih.
Pri sintezi piranoantocianov so kvasovke s sproščanjem metabolitov, prekurzorjev za nastanek vinilfenolnih piranoantocianov, zelo pomembne (Božič in sod., 2020a); prikazano na Sliki 2. Kvasovke z visoko aktivnostjo encima hidroksicinamatna dekarboksilaza (HCDC) lahko dekarboksilirajo fenolne spojine hidroksicimetne kisline v reaktivne vinilfenole, ki se kondenzirajo z antocianini, tako da nastanejo piranoantociani. Hidroksicimetne kisline p-kumarna, kavna, ferulna, sinapinska kislina lahko tudi neposredno reagirajo z antocianini, a ta mehanizem poteka počasi med staranjem vina (Suárez-Lepe in Morata, 2012).
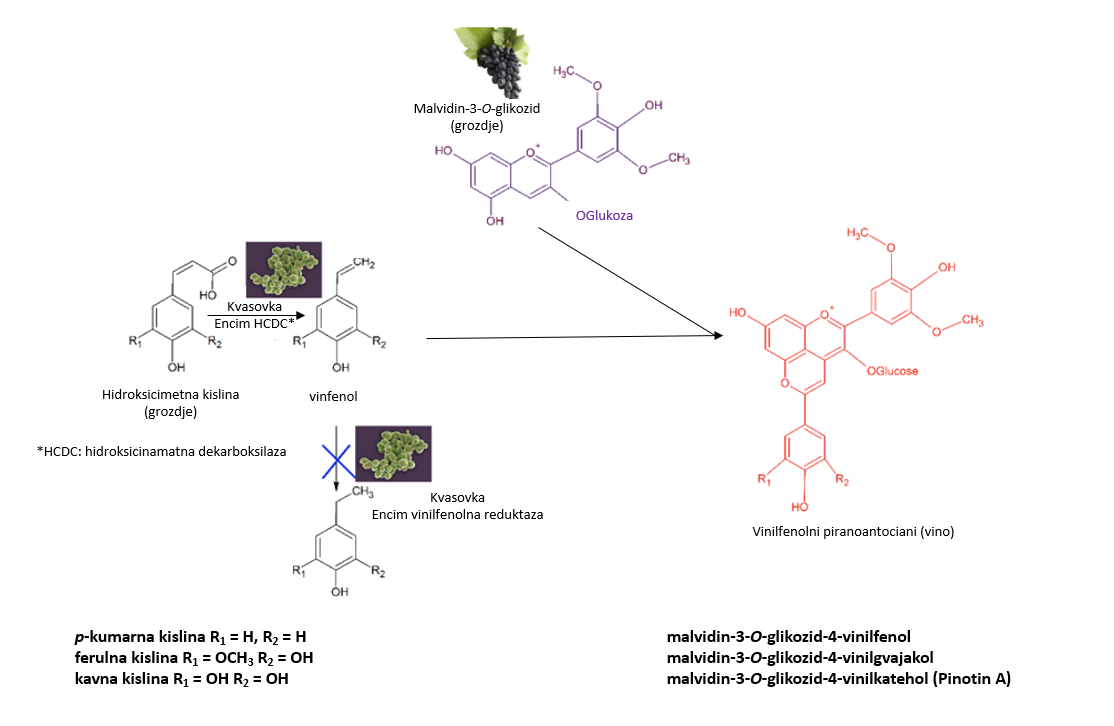
Kvasovke lahko pomembno pripomorejo tudi k izgubi barve vina. Sestava in poroznost celičnih sten fermentiranih kvasovk lahko povzroči znatno adsorpcijo hlapnih spojin oziroma adsorpcijo antocianinov na celične stene. Ta lastnost je še posebej pomembna pri sortah grozdja z manjšo vsebnostjo antocianov kot je modri pinot (Morata in sod., 2005).
Metode za določanje antocianov in piranoantocianov v vinu
Pri analizi fenolov in antocianov v vinu se uporabljata dva glavna pristopa. Prvi temelji na določanju skupne vrednosti monomernih antocianov z različnimi spektrofotometričnimi metodami. Drug pristop pa na uporabi separacijskih metod z različnimi sistemi za odkrivanje, kvantifikacijo in prepoznavanje antocianov in piranoantocianov v vinih in drugih matriksih.
Ključno pri analizi antocianov in piranoantocianov je ustrezna predpriprava vzorcev na analizo, ki mora imeti čim boljši izplen, čim bolje mora ponazarjati dejansko stanje v naravi, seveda pa mora biti tudi cenovno ustrezna glede na namen tovrstnih analiz vina.
Predpriprava vzorcev vključuje postopek čiščenja vzorcev in predkoncentracije zlasti pri določanju piranoantocianov, saj so ti prisotni v manjših koncentracijah v primerjavi z antociani in zaradi kompleksnosti vinskega matriksa, ki lahko prekrije spojine, v manjših koncentracijah. Najpogostejši metodi priprave vzorcev sta ekstrakcija tekoče-tekoče (LLE) in ekstrakcija na trdnem nosilcu (SPE). Poznamo več različnih pristopov, ki se razlikujejo v uporabi organskih topil in različnih sorbentov. Ekstrakcija na trdnem nosilcu omogoča večjo avtomatizacijo postopkov, hitrejšo obravnavo večjega števila vzorcev, in tudi enake pogoje ekstrakcij. Pri pripravi vzorcev vina se najpogosteje uporablja zgolj predhodna filtracija brez predhodne dodatne obdelave vzorcev (Aleixandre-Tudo in sod., 2017; Blanco-Vega in sod., 2014; He in sod., 2012a; Lorrain in sod., 2013).
Spektrofotometrične metode za določanje antocianov in piranoantocianov v vinu
Za določanje skupnih vrednosti monomernih antocianov se uporabljajo spektrofotometrične metode, naštete v nadaljevanju.
- Diferencialna metoda glede na pH
Metoda izhaja iz dejstva, da monomerni antociani reverzibilno spreminjajo strukturo in barvo v odvisnosti od pH-ja. Tako je razlika absorbance pigmentov pri 520 in 700 nm ter pri pH 1 in 4,5 proporcionalna koncentraciji antocianinov. Za preračunavanje v koncentracijo se uporablja molski ekstinkcijski koeficient antocianina (glavnega) v izbrani raztopini.
- Metoda s klorovodikovo kislino
Metoda se uporablja za oceno skupne vsebnosti antocianov. Vzorci vina se razredčijo v 1 M raztopini HCl. Čez čas (30 min) se izmeri absorbanco pri valovni dolžini 520 nm. Običajno se uporabijo 20- ali 50-kratne razredčitve. Koncentracije antocianov se izrazijo kot ekvivalenti malvidin-3-O-glikozida (mg/L).
- Metoda z uporabo razbarvanja z metabisulfitom (angl. Bisulfite bleaching method)
Metoda temelji na dveh kemijskih lastnostih antocianov: na odvisnosti od pH-ja in učinku razbarvanja. Metoda podaja kvantitativne informacije o skupni koncentraciji rdečih pigmentov. Pri tem upošteva lastnosti metabisulfita, ki ga ima na barvne pigmente. Antociane razbarva, medtem ko se polimerni pigmenti ne razbarvajo, ker so odpornejši na razpadanje v prisotnosti SO2. Absorbanca vzorca, ki se tretira z bisulfitom, se primerja z absorbanco netretiranega vzorca pri 520 nm. Antociani so izraženi kot ekvivalenti malvidin-3-O-glikozida (mg/L). Metoda poda informacije o skupni vsebini monomernih antocianov ob odštetju polimerne frakcije (Aleixandre-Tudo in sod., 2017; Giusti and Wrolstad, 2001). Piranoantociana, kot sta vitizin A in vitizin B, se ob prisotnosti bisulfita ne razbarvata in sta izražena kot polimerna barva. Po tej metodi lahko rezultati pokažejo preveliko koncentracijo antocianov, ker na nekatere polimerne pigmente vpliva tudi učinek razbarvanja (bolj izraženo v mladih vinih). Pri staranju vin nastanejo kompleksnejši pigmenti, ki so manj občutljivi za SO2 (Aleixandre-Tudo in sod., 2017).
Separacijske metode za določanje antocianov in piranoantocianov v vinu
Tekočinska kromatografija visoke ločljivosti (HPLC) je najpogosteje uporabljena analizna tehnika za ločevanje in separacijo ter prepoznavanje polifenolnih spojin grozdja in vina, med njimi tudi antocianov. Pri tem se uporabljajo različni detektorji: masni spektrometer (MS), detektor na niz diod (DAD), UV-VIS detektor. Najpogosteje se pri potrjevanju uporabijo podatki vseh detektorjev, zlasti če standardne spojine niso dostopne na trgu.
Trenutno ni enotne kromatografske tehnike, ki bi lahko ločila različne skupine fenolnih spojin z eno kromatografsko analizo. Zato moramo, če želimo celoten profil fenolnih spojin, optimizirati izbor stacionarne faze, mobilne faze, gradientno elucijo, temperaturo in hitrost pretoka mobilne faze. Običajno se ločevanje fenolnih skupin izvaja z reverznofazno kromatografijo, pri kateri se uporabita nepolarna stacionarna faza in polarna mobilna faza (López-Fernández in sod., 2020). Polifenolne spojine grozdja in vina se med seboj razlikujejo v polarnosti, tako da pri reverznofazni kromatografiji iz kolone najprej eluirajo najbolj polarne spojine in nazadnje najmanj polarne spojine. Vrstni red teh spojin je bil že večkrat omenjen in ga lahko najdemo v literaturi – lahko nam tudi pomaga pri prepoznavanju fenolnih spojin grozdja in vina (Kalogiouri in sod., 2022).
Kombinacija, ki se danes najpogosteje uporablja za določanje profila antocianov, je tekočinska kromatografija visoke ločljivosti z detektorji na niz diod (DAD detektor), masnim spektrometrom (MS) ali tandemsko masno spektrometrijo (MS/MS) (He in sod., 2012a; Lorrain in sod., 2013). Pri uporabi DAD detektorja prepoznavanje spojin temelji na merjenju UV-VIS spektra spojine, retencijskega časa ter na primerjavi z retencijskim časom in UV-VIS spektrom analitskega standarda. Glavna pomanjkljivost DAD detektorja je nezmožnost razlikovanja med spojinami, ki imajo podobne spektroskopske značilnosti, čeprav lahko na podlagi spektrov v UV in VIS območju antocianine ločimo od flavonolov, flavan-3-olov in fenolnih kislin. Težavno je tudi razlikovanje med spojinami, ki koeluirajo pod izbranimi kromatografskimi pogoji. Kvantifikacija antocianinov poteka z eksterno kalibracijo z antocianinom samim, če je standardna spojina tržno dostopna, drugače pa antocianine lahko izražamo kot ekvivalente glavnega antocianina grozdja in vina, to je malvidin-3-O-glukozid. Na sliki 3 sta prikazana kromatograma vina modri pinot na dan stekleničenja (A) in po treh mesecih staranja (B). Prikazana sta UV-VIS spektra malvidin-3-O-glikozida (spojina je označena s številko 1) in piranoantociana malvidin-3-O-glikozid-4-vinilkatehola (spojina, označena s številko 2). Za malvidin-3-O-glikozid-4-vinilkatehol so prikazani tudi MS, MS2 in MS3 spektri, saj komercialni standardi niso na voljo za prepoznavanje. Pri UV-VIS spektru piranoantocianov je viden ožji absorpcijski vrh, prav tako valovna dolžina, pri čemer je maksimalna absorpcija premaknjena, saj je absorpcijski vrh pri malvidin-3-O-glikozid-4-vinilkateholu 509 nm, medtem ko je pri malvidin-3-O-glikozidu 526 nm (Božič in sod., 2020b).
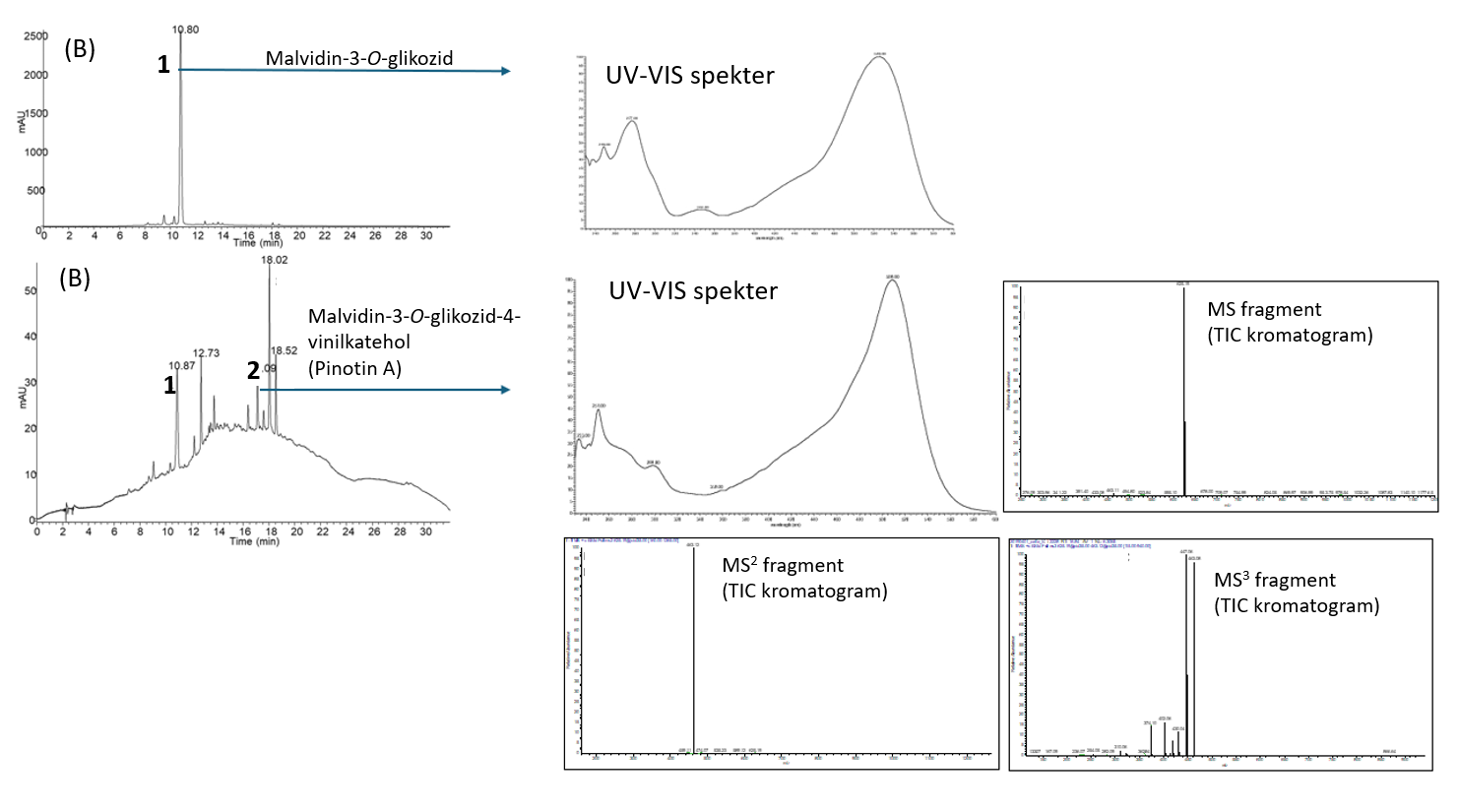
Uporaba HPLC-DAD metod pri prepoznavanju piranoantocianov je zelo omejena, saj komercialni analizni standardi niso na voljo. Za poglobljenejšo analizo antocianov in piranoantocianov se uporablja HPLC skupaj z masno spektrometrijo (MS) ali tandemsko masno spektrometrijo (MS/MS), ki omogočata prepoznavanje in kvantifikacijo analitov v vzorcu ali potrditev molekulske strukture. MS temelji na ločevanju analitov glede na njihovo razmerje med maso in nabojem (m/z). Poleg metode HPLC se za separacijo antocianov in piranoantocianov uporablja tudi tekočinska kromatografija ultravisoke ločljivosti (UPLC). V primerjavi s HPLC-jem so analize krajše, manjša je tudi poraba topil (Blanco-Vega in sod., 2014; Dipalmo in sod., 2016; Lorrain in sod., 2013; Valls in sod., 2009).
Določanje barve vina
Spektrofotometrična analiza
Barvo vina določamo z merjenjem absorbance svetlobe pri določenih valovnih dolžinah, običajno v območju od 400 do 700 nm. Spektrofotometer pošlje svetlobo skozi vzorec filtriranega vina, absorbanco (koliko svetlobe vino absorbira) pa merimo pri različnih valovnih dolžinah. Če je pri rdečih vinih absorbanca vzorca prevelika (večja od 1 AU), je treba vzorec redčiti s pufrom, ki ima pH enak pH-ju vina, ali pa uporabimo kiveto s krajšo optično potjo (1 mm namesto 10 mm). Za rdeča vina se običajno uporabljajo tri ključne valovne dolžine (OIV, 2019):
420 nm: za rumenkaste odtenke,
520 nm: za rdečkaste odtenke,
620 nm: za modrikaste odtenke.
S seštevkom absorbanc vseh treh valovnih dolžin dobimo parameter intenzivnost, z razmerjem med absorbanco 420 nm in 520 nm pa parameter, ki ga imenujemo odtenek (hue). Metoda je enostavna, hitra in ponovljiva. Primerna je za rutinsko uporabo in omogoča primerjavo med različnimi vzorci vin. Vendar pa ne upošteva kompleksnosti zaznavanja barve, saj jo določa samo na podlagi absorbance pri določenih valovnih dolžinah. Prav tako ne zagotavlja podatkov o barvnem tonu in nasičenosti (OIV, 2019).
Metoda CIE Lab
CIE Lab je barvni prostor, ki temelji na človekovem zaznavanju barve. Vzpostavila ga je Mednarodna komisija za osvetlitev (CIE) leta 1976. Barva je opredeljena s tremi koordinatami:
L*: svetlost oziroma temnost (0 = črna, 100 = bela);
a*: zeleno-rdeča os (negativne vrednosti = zelena, pozitivne vrednosti = rdeča);
b*: modro-rumena os (negativne vrednosti = modra, pozitivne vrednosti = rumena) (CIE, 2007).
Barva vzorca vina se izmeri s spektrofotometrom ali kolorimetrom, ki podatke pretvori v vrednosti L*, a* in b*. Te vrednosti omogočajo tridimenzionalno predstavitev barve vina, kar omogoča natančno in objektivno primerjavo med različnimi vini (Hunter and Harold, 1987; Wrolstad, 2005).
Metoda CIE Lab ponuja popolno sliko barve, vključno s svetlostjo, nasičenostjo in odtenkom. Omogoča natančno kvantifikacijo barvnih razlik, kar je pomembno za kakovostno kontrolo in raziskave. Zahteva bolj sofisticirano opremo in je nekoliko bolj zapletena za izvedbo v primerjavi s klasično spektrofotometrijo. Poleg tega je dražja (Hunter and Harold, 1987; Wrolstad, 2005).
Primerjava metode CIE Lab in klasične spektrofotometrije
Natančnost in kompleksnost. CIE Lab je bistveno natančnejša in upošteva celotno spektralno zaznavanje barve, medtem ko klasična spektrofotometrija meri le intenziteto svetlobe pri določenih valovnih dolžinah.
Stroški in zahtevnost. Klasična metoda je cenejša in lažja za izvedbo, medtem ko je CIE Lab zapletenejša in dražja, vendar ponuja podrobnejše podatke.
Uporaba v praksi. Spektrofotometrija je še vedno široko uporabljena v rutinskih analizah zaradi enostavnosti in stroškovne učinkovitosti, medtem ko se CIE Lab uporablja v raziskavah in za visokokakovostno kontrolo, kjer je potrebna natančna analiza barve (Hunter in Harold, 1987; Wrolstad, 2005).
Vaja
Določanje profila antocianov v grozdju in vinu
Priprava vzorcev
Določanje profila antocianov v grozdnih kožicah
Grozdne kožice ločimo od pešk in pulpe ter jih liofiliziramo do suhega. Tako pripravljene zmeljemo v terilnici do homogenega vzorca. Tako pripravljen 1 g zmletih in liofiliziranih kožic zmešamo z 20 mL metanola (MeOH) čistoče HPLC in postavimo v ultrazvočno kopel za 15 min na stresanje. Uporabimo polietilensko centrifugirko. Sledi centrifugiranje (4 °C, 5 min, 5000 vrt./min). Postopek ekstrakcije se ponovi štirikrat, pri čemer ločeno zbiramo supernatant, sediment pa ponovno izpostavimo ekstrakciji z metanolom v ultrazvočni kopeli.
Supernatant zbiramo in v tako pripravljenem vzorcu odstranimo metanol z odparevanjem v vakuumskemu izparilniku pri 35 °C do suhega preostanka. Ekstrakt antocianov iz kožic grozdja ponovno raztopimo v natančno odmerjenem volumnu mobilne faze A (kisla mobilna faza) metode HPLC in ga filtriramo v viale z 0,45-µm PTFE filtrom. Vzorec je tako pripravljen za analizo HPLC-DAD.
Protokol ekstrakcije fenolnih spojin iz liofiliziranih kožic grozdja:
- V 50-ml centrifugalno epruveto (polietilensko) natehtamo 1 g liofiliziranih kožic grozdja.
- Dodamo 20 mL MeOH (HPLC čistoče).
- Ultrazvočna kopel 15 min.
- Centrifuga: 5 min, 5000 vrt./min (nizka temperatura)
- Zberemo supernatant v čašo/steklenico.
- Postopek ponovimo še 3-krat.
- Supernatante dopolnimo do 100 mL z metanolom
- Vzamemo alikvot vzorca ter prenesemo v 4-ml viale za shranjevanje. Shranimo pri –20 °C.
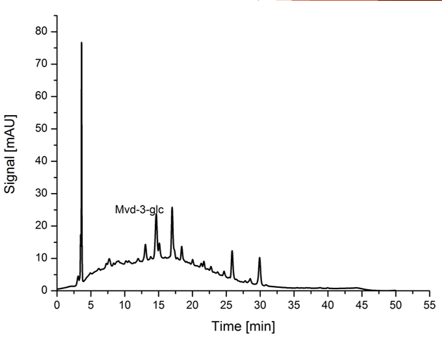
Analiza vin – neposredno injiciranje
Pri tovrstni analizi vina nimamo predpriprave s prečiščenjem in koncentriranjem analitov. Kromatogrami bodo zaradi tega malce grši, ampak še vedno dovolj dobri, da iz njih razberemo podatke o vrhovih polifenolov ter njihovih retencijskih in spektralnih karakteristikah. Takšno analizo lahko izvedemo le pri analizi HPLC-DAD in ob kombinaciji predkolone s kolono. Vzorce vina pred analizo HPLC-MS moramo vedno prečistiti z ekstrakcijo na trdnem nosilcu (SPE). Vzorec filtriramo skozi 0,45-µm PTFE filter in analiziramo z analizo HPLC-DAD. Tudi pred LC-MS analizo ni vedno potrebna priprava vzorca, je pa ta priporočljiva, da se zmanjšajo morebitni matrični efekti, ki vplivajo na kvantitativno analizo in da se odstrani morebitne delce iz vzorca ali pa če je potrebno koncentriranje oz. redčenje vzorca. Na Sliki 4 je prikazan primer neposrednega injiciranja vzorca.
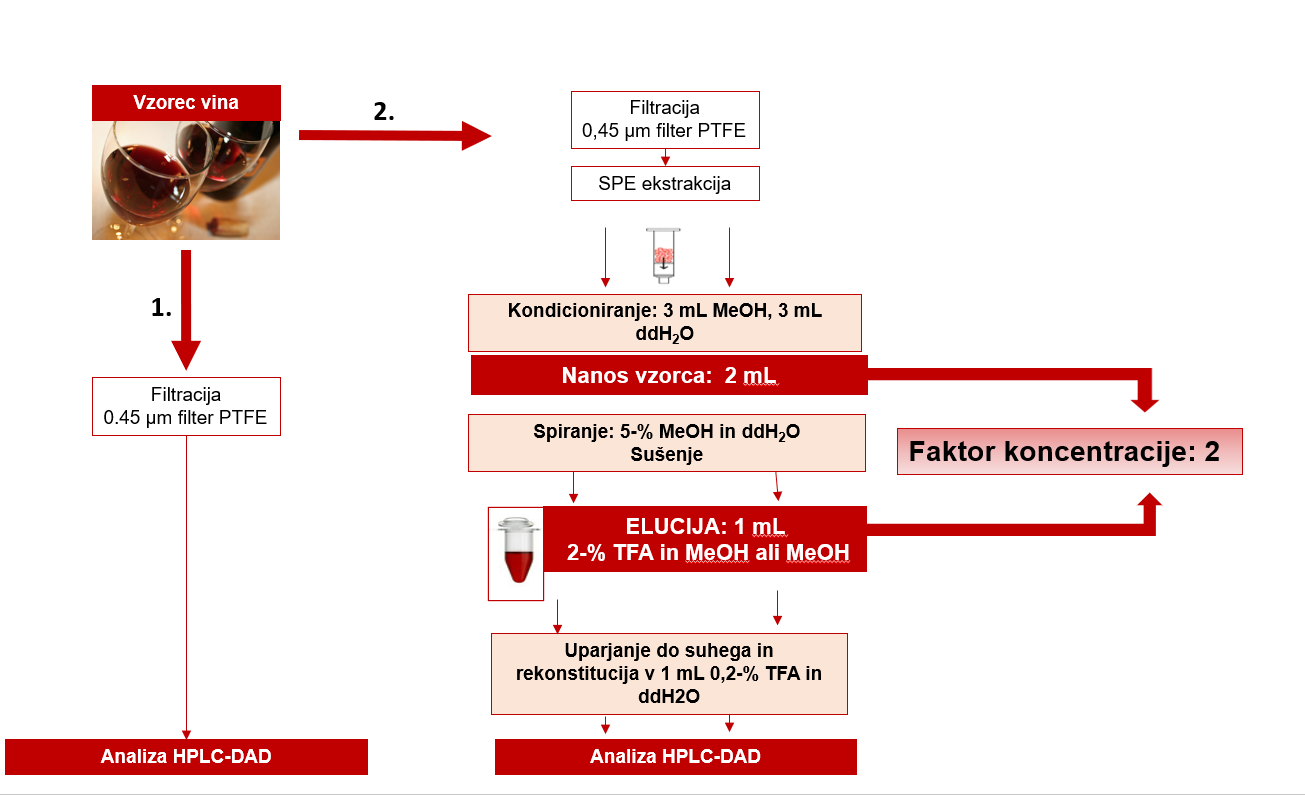
Analiza vina – ekstrakcija na trdem nosilcu
Zaradi kompleksnosti vinske matrice je včasih potrebna ekstrakcija SPE. Njen namen je čiščenje in predkoncentriranje vzorcev, kar je pomembno zlasti pri analizi spojin, prisotnih v manjših koncentracijah (piranoantociani).
Protokol ekstrakcije na trdni fazi (povzeto po Topić in sod. 2017):
- Pripravimo 5-% (v/v) MeOH v ddH2O.
- Kondicioniranje kartuš SPE-ja (HLB 6 mg, Waters) s 3 ml MeOH in 3 ml ddH2O (pomembno je, da vse raztopine na kolonice SPE dodajamo počasi – pretok uravnavamo tako, da se tekočine izmenjujejo na koli s kapljicami). Pri tem si lahko pomagamo s pritiskanjem tekočine s pomočjo tlaka (ročno) ali podtlaka z uporabo t. i. manifolda, ki je prikazan na Sliki 5.
- Počasi dodajamo 2 mL vzorca vina (filtriranega).
- Speremo nečistoče iz vzorca na kartuši s 5-% (v/v) MeOH, eluent zavržemo.
- Osušimo kartušo z uporabo tlaka (ročno) ali podtlaka z uporabo t.i. manifolda, ki je prikazan na Sliki 5 (če to izvajamo ročno, enostavno z brizgo večkrat potisnemo zrak skozi kartušo).
- Izperemo/eluiramo fenolne spojine z 1 ml MeOH v vialo.
- Tako pripravljen ekstrakt v MeOH posušimo do suhega (v izparilniku ali s protitokom dušika) in suhi preostanek raztopimo ponovno v 1 mL mobilne faze A analize HPLC. Nastavek za sušenje, ki se poveže s tokom dušika, je prikazan na Sliki 6.
Shematski prikaz protokola ekstrakcije na trdnem nosilcu je prikazan na Sliki 7.


Analiza HPLC-DAD
Za analizo HPLC-DAD se največkrat uporabljajo metode z ločbo na koloni C18. Kolone so različne, ki ločijo spojine po polarnosti. Ločba je odvisna tudi od drugih mehanizmov, ki pa so odvisni od tipa kolone. V tem poglavju opisujemo analizno metodo s kromatografsko kolono Kinetex EVO C18 (250 x 4,6 mm, 5 µm id) z ujemajočo se predkolono (Phenomenex, Torrance, ZDA) (Božič in sod., 2020a).
Za izvedbo analize najprej pripravimo mobilno fazo A, in sicer tako, da raztopimo 2,2-% HPLC grade mravljične kisline (v/v) v dvakrat deionizirani vodi (ddH2O). Mobilna faza B je sestavljena iz 2,2 % mravljične kisline, 85 % acetonitrila (ACN, HPLC stopnja čistoče), 12,8 % ddH2 O (v/v). Prenesemo 50 mL mobilne faze A v vialo za shranjevanje – da se pripravijo delovne raztopine. Osnovna standardna raztopina je zaradi stabilnosti pripravljena v MeOH.
Iz predhodno pripravljene osnovne raztopine malvidin-3-O-glikozida (100 mg/L) v MeOH pripravimo delovne raztopine umeritvene krivulje. Vse standardne raztopine antocianov pripravljamo v MeOH in shranjujemo tesno zaprte v zmrzovalniku. Tako ostanejo spojine dolgo nespremenjene. Če bi jih shranjevali v kislih raztopinah, se sčasoma razgradijo glikozidne vezi.
Delovne raztopine za umerjanje koncentracije antocianov v naših vzorcih pripravimo v območju 1–500 mg/L (1 mg/L, 5 mg/L, 10 mg/L, 50 mg /L, 100 mg/L, 250 mg/L, 500 mg/L). Vse raztopine so pripravljene v MeOH in tako prenesene v viale HPLC, ki so potem izpostavljene uparjanju do suhega, čemur sledi rekonstitucija suhega preostanka v mobilni fazi A. Rekonstrukcijo suhih preostankov naredimo v istem volumnu kot vzorce. Če je drugače, si zapomnimo, ker je pomembno pri preračunavanju koncentracij fenolnih spojin.
Potem ko pripravimo vzorce standardnih raztopin, prenesemo alikvot ekstrakta fenolov grozdnih kožic (500 µL) v vialo HPLC in odparimo do suhega, tako kot smo to naredili pri standardnih raztopinah (lahko uporabimo avtomatski izparilec ali protitok dušika). Na Sliki 6 je primer nastavka za sušenje, ki se poveže s tokom dušika. Za sušenje se lahko uporablja tudi sistem MultiVac.
Suhi preostanek vzorca ponovno raztopimo v 500 µL mobilne faze A. Tako pripravljen vzorec analiziramo s HPLC-DAD.
Tabela 2. HPLC pogoji kromatografske analize.
|
Sistem HPLC |
Agilent 1200/Agilent 1100 (lahko je tudi kromatografski sistem drugega proizvajalca) |
|
Kromatografska kolona |
Kinetex EVO (250 x 4,6 mm, 5 µm) |
|
Temperatura kolone |
40 °C |
|
Mobilna faza A |
2,2 % mravljična kislina v ddH2O |
|
Mobilna faza B |
2,2 % mravljična kislina, 85 % ACN, 12,8 % ddH 2 O |
|
Gradient |
Gradient: 0 min 100 % A, 0–5 min 10 % B, 5–20 min 10–35 % B, 20–22 min 35 % B, 22–26 min 35–45 % B, 26–27 min 45–60 % B, 27–32 min 100 A |
|
Pretok |
1 ml/min |
|
Detektor |
520 nm |
|
Volumen injiciranja |
20 µL |
Iz standardnih raztopin pripravimo umeritveno krivuljo v programu za izračun premice. Površine spojin, ki smo jih prepoznali kot antocianine ali piranoantociane, preračunamo v koncentracije v mg/L, pri čemer upoštevamo morebitne redčitvene faktorje. Pri analizi vina podajamo rezultate v mg/L vina, medtem ko nas pri kožicah zanima mg/kg ali g suhih kožic. Za vinogradnika in vinarja je sicer najbolj praktičen rezultat na kg grozdnih jagod. Če bi želeli preračunati na svežo maso jagod, potem bi morali upoštevati natančno količino mase kožic na kg jagod, in tudi izgubo vode v procesu liofiliziranja. To določimo s tehtanjem vzorcev pred samimi koraki predpriprave biološkega vzorca grozdnih jagod.
Za natančne analize je treba vse postopke, ki so vir napake, ponavljati vsaj trikrat in določiti napako. Najmanjšo napako ima sama kromatografska analiza. Pri podajanju rezultatov je pomemben podatek, za kakšne ponovitve gre v samem rezultatu – ali gre za ponovitev injiciranja ali ekstrahiranja, ali pa že biološkega vzorca iz vinograda, ki naj ima najmanj 100 jagod.
Protokol za merjenje barve vin
Barva rdečega vina se lahko določi z UV-VIS spektrofotometrom. Uporabimo kiveto z dolžino optične poti 1 mm. Vzorec filtriramo skozi 0,45-µm filter in odpipetiramo 500 µL. Izmerimo absorbanco pri treh različnih dolžinah (420, 520 in 620 nm) v skladu z metodologijo OIV (OIV, 2019).
Intenzivnost barve izračunamo kot vsoto absorbanc pri 420, 520 in 620 nm.
Odtenek vina izračunamo kot razmerje med absorbancama pri 420 in 520 nm.
Viri
Alcalde-Eon, C., Escribano-Bailón, M. T., Santos-Buelga, C., Rivas-Gonzalo, J. C. 2006. Changes in the detailed pigment composition of red wine during maturity and ageing. Anal. Chim. Acta 563, 238–254. https://doi.org/10.1016/j.aca.2005.11.028
Aleixandre-Tudo, J. L., Buica, A., Nieuwoudt, H., Aleixandre, J. L., du Toit, W. 2017. Spectrophotometric Analysis of Phenolic Compounds in Grapes and Wines. J. Agric. Food Chem. 65, 4009–4026. https://doi.org/10.1021/acs.jafc.7b01724
Blanco-Vega, D., Gómez-Alonso, S., Hermosín-Gutiérrez, I. 2014. Identification, content and distribution of anthocyanins and low molecular weight anthocyanin-derived pigments in Spanish commercial red wines. Food Chem. 158, 449–458. https://doi.org/10.1016/j.foodchem.2014.02.154
Boulton, R. B., Singleton, V. L., Bisson, L. F., Kunkee, R. E. 2013. Principles and Practices of Winemaking. Springer Science & Business Media.
Božič, J. T., Butinar, L., Albreht, A., Vovk, I., Korte, D., Vodopivec, B. M. 2020a. The impact of Saccharomyces and non-Saccharomyces yeasts on wine colour: A laboratory study of vinylphenolic pyranoanthocyanin formation and anthocyanin cell wall adsorption. LWT 123, 109072. https://doi.org/10.1016/j.lwt.2020.109072
Božič, J. T., Ćurko, N., Ganić, K. K., Butinar, L., Albreht, A., Vovk, I., Korte, D., Vodopivec, B. M. 2020b. Synthesis of pyranoanthocyanins from Pinot Noir grape skin extract using fermentation with high pyranoanthocyanin producing yeasts and model wine storage as potential approaches in the production of stable natural food colorants. Eur. Food Res. Technol. 1–12. https://doi.org/10.1007/s00217-020-03467-2
Champ, C. E., Kundu-Champ, A. 2019. Maximizing Polyphenol Content to Uncork the Relationship Between Wine and Cancer. Front. Nutr. 6.
CIE. 2007. Colorimetry-part 4: CIE 1976 L* a* b* colour space. Int. Stand. 2019–06.
Dipalmo, T., Crupi, P., Pati, S., Clodoveo, M.L., Di Luccia, A., 2016. Studying the evolution of anthocyanin-derived pigments in a typical red wine of Southern Italy to assess its resistance to aging. LWT – Food Sci. Technol. 71, 1–9. https://doi.org/10.1016/j.lwt.2016.03.012
Freitas, V.A.P. de, Fernandes, A., Oliveira, J., Teixeira, N., Mateus, N. 2017. A review of the current knowledge of red wine colour. OENO One 51. https://doi.org/10.20870/oeno-one.2017.51.1.1604
Giusti, M. M., Wrolstad, R. E. 2001. Characterization and Measurement of Anthocyanins by UV-Visible Spectroscopy. Curr. Protoc. Food Anal. Chem. 00, F1.2.1-F1.2.13. https://doi.org/10.1002/0471142913.faf0102s00
He, F., Liang, N.-N., Mu, L., Pan, Q.-H., Wang, J., Reeves, M.J., Duan, C.-Q. 2012a. Anthocyanins and Their Variation in Red Wines I. Monomeric Anthocyanins and Their Color Expression. Molecules 17, 1571–1601. https://doi.org/10.3390/molecules17021571
He, F., Liang, N.-N., Mu, L., Pan, Q.-H., Wang, J., Reeves, M.J., Duan, C.-Q. 2012b. Anthocyanins and Their Variation in Red Wines II. Anthocyanin Derived Pigments and Their Color Evolution. Molecules 17, 1483–1519. https://doi.org/10.3390/molecules17021483
He, F., Mu, L., Yan, G.-L., Liang, N.-N., Pan, Q.-H., Wang, J., Reeves, M.J., Duan, C.-Q. 2010. Biosynthesis of Anthocyanins and Their Regulation in Colored Grapes. Molecules 15, 9057–9091. https://doi.org/10.3390/molecules15129057
Hunter, R. S., Harold, R. W. 1987. The Measurement of Appearance. John Wiley & Sons.
Kalogiouri, N. P., Karadimou, C., Avgidou, M. S., Petsa, E., Papadakis, E.-N., Theocharis, S., Mourtzinos, I., Menkissoglu-Spiroudi, U., Koundouras, S. 2022. An Optimized HPLC-DAD Methodology for the Determination of Anthocyanins in Grape Skins of Red Greek Winegrape Cultivars (Vitis vinifera L.). Molecules 27, 7107. https://doi.org/10.3390/molecules27207107
López-Fernández, O., Domínguez, R., Pateiro, M., Munekata, P. E. S., Rocchetti, G., Lorenzo, J. M. 2020. Determination of Polyphenols Using Liquid Chromatography–Tandem Mass Spectrometry Technique (LC–MS/MS): A Review. Antioxidants 9, 479. https://doi.org/10.3390/antiox9060479
Lorrain, B., Ky, I., Pechamat, L., Teissedre, P.-L. 2013. Evolution of Analysis of Polyhenols from Grapes, Wines, and Extracts. Molecules 18, 1076–1100. https://doi.org/10.3390/molecules18011076
Macheix, J.-J. 2017. Fruit Phenolics. CRC Press, Boca Raton. https://doi.org/10.1201/9781351072175
Merecz-Sadowska, A., Sitarek, P., Kowalczyk, T., Zajdel, K., Jęcek, M., Nowak, P., Zajdel, R. 2023. Food Anthocyanins: Malvidin and Its Glycosides as Promising Antioxidant and Anti-Inflammatory Agents with Potential Health Benefits. Nutrients 15, 3016. https://doi.org/10.3390/nu15133016
Minnaar, P., Nyobo, L., Jolly, N., Ntushelo, N., Meiring, S. 2018. Anthocyanins and polyphenols in Cabernet Franc wines produced with Saccharomyces cerevisiae and Torulaspora delbrueckii yeast strains: Spectrophotometric analysis and effect on selected sensory attributes. Food Chem. 268, 287–291. https://doi.org/10.1016/j.foodchem.2018.06.074
Morata, A., Gómez-Cordovés, M. C., Colomo, B., Suárez, J. A. 2005. Cell wall anthocyanin adsorption by different Saccharomyces strains during the fermentation of Vitis vinifera L. cv Graciano grapes. Eur. Food Res. Technol. 220, 341–346. https://doi.org/10.1007/s00217-004-1053-8
Moreno, J., Peinado, R. 2012. Enological Chemistry. Academic Press.
Nikfardjam, M. S. P., Márk, L., Avar, P., Figler, M., Ohmacht, R. 2006. Polyphenols, anthocyanins, and trans-resveratrol in red wines from the Hungarian Villány region. Food Chem. 98, 453–462. https://doi.org/10.1016/j.foodchem.2005.06.014
OIV. 2019. OIV – Compendium of International Methods of Analysis of Wines and Musts (2 vol.). International Organisation of Vine and Wine.
Panche, A. N., Diwan, A. D., Chandra, S. R. 2016. Flavonoids: an overview. J. Nutr. Sci. 5, e47. https://doi.org/10.1017/jns.2016.41
Sabra, A., Netticadan, T., Wijekoon, C. 2021. Grape bioactive molecules, and the potential health benefits in reducing the risk of heart diseases. Food Chem. X 12, 100149. https://doi.org/10.1016/j.fochx.2021.100149
Suárez-Lepe, J. A., Morata, A. 2012. New trends in yeast selection for winemaking. Trends Food Sci. Technol. 23, 39–50. https://doi.org/10.1016/j.tifs.2011.08.005
Topić, J., Korte, D., Mozetič Vodopivec, B. 2017. The comparison of anthocyanin and pyranoanthocyanin extraction efficiency in Pinot Noir wine using SPE. V: Book of abstracts 24th young Investigators Seminar on Analytical Chemistry. Venice, Italy.
Topić Božič, J., Butinar, L., Antalick, G., Sternad Lemut, M., Martelanc, M., Albreht, A., Korte, D., Mozetič Vodopivec, B. 2022. The influence of selected indigenous yeasts on Pinot Noir wine colour properties. J. Sci. Food Agric. 102, 664–672. https://doi.org/10.1002/jsfa.11395
Topić Božič, J., Korte, D., Butinar, L., Mozetič Vodopivec, B., 2019. Yeasts and wine colour. Croat. J. Food Sci. Technol. 11, 291–302. https://doi.org/10.17508/CJFST.2019.11.2.17
Valls, J., Millán, S., Martí, M.P., Borràs, E., Arola, L. 2009. Advanced separation methods of food anthocyanins, isoflavones and flavanols. J. Chromatogr. A, Advanced Separation Methods in Food Analysis 1216, 7143–7172. https://doi.org/10.1016/j.chroma.2009.07.030
Waterhouse, A. L. 2002. Wine Phenolics. Ann. N. Y. Acad. Sci. 957, 21–36. https://doi.org/10.1111/j.1749-6632.2002.tb02903.x
Waterhouse, A. L., Sacks, G. L., Jeffery, D. W. 2016. Understanding Wine Chemistry, Understanding Wine Chemistry. John Wiley & Sons, Ltd. https://doi.org/10.1002/9781118730720
Welch, C. R., Wu, Q., Simon, J. E. 2008. Recent Advances in Anthocyanin Analysis and Characterization. Curr. Anal. Chem. 4, 75–101.
Wrolstad, R. E. 2005. Current Protocols in Food Analytical Chemistry. John Wiley.
