5 Polifenoli belega grozdja in vina
Branka Mozetič Vodopivec and Magdalina Mihajlovska
Uvod
Polifenoli so kemijske spojine, ki jih najdemo v številnih živilih in pijačah, pa tudi v grozdju in vinu. Zaradi svoje edinstvene kemične strukture pomembno vplivajo na senzorične lastnosti vina in imajo možnosti za staranje vina in imajo koristi za zdravje ljudi. Belo grozdje ima manj polifenolov kot rdeče grozdje in ponavadi nič antocianinov, in če že, pa so to zelo, zelo majhne koncentracije (Panagiotis in sod., 2015), ki se v prvih fazah predelave grozdja večinoma oksidirajo, ali porazgubijo, in jih je v vinih enostavno lahko premalo za detekcijo – tako instrumentalno kot tudi senzorično.
Tabela 1: Povprečne vsebnosti flavonoidnih fenolnih spojin v belem grozdju (povzeto po Clark in sod., 2022).
|
Vrsta flavonola |
Vrsta |
Vir |
Koncentracija |
|
Flavan-3-oli |
(+) katehin (-) epikatehin (-) epikatehin galat (-) epigalokatehin Procianidini Kondenzirani tanini |
Kožice Peške |
Monomernih je 15-25 mgL-1 20-25 mgL-1pa polimernih |
|
Flavonoli |
Kvercitin Kamferol Mircetin (kot glukozidi najpogosteje) |
Kožice |
Majhne koncentracije |
|
Antocianini |
Cianidinin-3-glukozid Delfinidin-3-glikozid Petunidin-3-glukozid Peonidin-3-glukozid Malvdiin-3-glukozid |
Rdeča barvila v kožicah belega grozdja |
Sledovi |
Polifenoli so znani po svojih močnih antioksidativnih lastnostih, ki so bistvene za nevtralizacijo prostih radikalov in blažitev oksidativnega stresa, povezanega s staranjem in boleznimi pri človeku. Izkazujejo močne protivnetne učinke, ki so ključnega pomena pri odpravljanju kroničnega vnetja, ki je prevladujoč dejavnik številnih kroničnih bolezni. Polifenoli prispevajo k zdravju srca in ožilja, saj izboljšujejo krvni obtok, zmanjšujejo krvni tlak in podpirajo žilne funkcije (Lucarini in sod., 2021). Poleg tega njihove protimikrobne lastnosti pomagajo pri imunskem sistemu in potencialno ščitijo pred okužbami (Gutiérrez-Escobar in sod., 2021). Polifenoli imajo lahko tudi nevroprotektivne prednosti, saj spodbujajo zdravje in delovanje možganov, kar poudarja njihove celovite koristi za zdravje v rdečih in belih vinih, če jih zmerno uživamo (Lucarini in sod., 2021).
Če primerjamo celokupno vsebnost fenolnih spojin imajo rdeča vina v povprečju 215 mg/100 mL skupnih fenolov (kot galna kislina), bela v povprečju 32 mg/100 mL in rose vina 82 mg/100 mL (Rothwell in sod., 2013).
Kemijske strukture in opisi skupin fenolov
Polifenoli so skupina spojin, ki jih najdemo v različnih rastlinah in veljajo za sekundarne metabolite. V kemiji vina in grozdja so polifenoli spojine, ki vsebujejo vsaj en fenolni obroč s hidroksilno skupino (Slika 1).
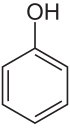
Slika 1: Osnovna kemijska struktra fenola.
V grozdju so polifenoli razporejeni po vsej jagodi, pri čemer prevladujejo predvsem v različnih delih grozdne jagode, kot so kožice, pečke ali pulpa. Koncentrirani so predvsem v kožici in peškah grozdnih jagod, pri čemer so njihove vsebnosti običajno večje v rdečem grozdju in vinih v primerjavi z belim grozdjem (Moreno in Peinado, 2012, Rothwell in sod., 2013, Waterhouse in sod., 2016).
Tabela 2: Razdelitev polifenolov v sadju z glavnimi predstavniki (Macheix in sod., 1990)
|
Število C atomov |
Osnovni skelet |
Razred |
Primer spojine |
|
7 |
C6-C1 |
Hidroksibenzojske kisline |
p–hidroksibenzojska kislina |
|
9 |
C6-C3 |
Hidroksicimetne kisline, Kumarini |
Kavna kislina Skopolin |
|
10 |
C6-C4 |
Naftokinoni |
Juglon |
|
13 |
C6-C1-C6 |
Ksantoni |
Mangiferin |
|
14 |
C6-C2-C6 |
Stilbeni |
Resveratrol |
|
15 n
|
C6-C3-C6 |
Flavonoidi Izoflavonoidi Lignini Tanini |
Kvercetin, cianidin Daidzein |
Ne glede na to, da jih je v belih vinih manj kot v rdečih vinih, tudi tu prispevajo pomembno k videzu vina, in tudi okusu vina – koliko, pa je odvisno predvsem od metode pridelave vina, in še posebej, če le-ta vsebuje podaljšani kontakt s kožicami in pečkami, pred fermentacijo ali med fermentacijo, lahko pa tudi po fermentaciji.
Fenolne spojine so prisotne vsepovsod v naravi, obstaja več klasifikacij, najpogostejša pa je tista po številu C atomov v strukturi (Tabela 2).
V belem grozdju seveda nimamo vseh skupin fenolov, ki so navedeni v Tabeli 1, le nekatere predstavnike. Glavna delitev fenolov v grozdju – glede na njihovo kemijsko zgradbo, je na:
- Flavonoidne (difenilpropanoide) in
- Neflavonoidne (fenilpropanoide) polifenole.
Flavonoidi imajo skelet iz 15 ogljikovih atomov, ki so organizirani v dva fenolna obroča (A in B), ki sta povezana preko vmesnega heterocikla (C). Te spojine imajo v glavnem strukturo, ki jo na kratko opišemo z C6-C3-C6 (Macheix in sod., 1990).
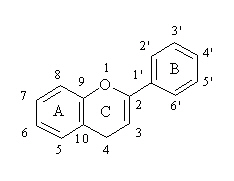
Slika 2: Osnovna strukturna formula flavonoidov; 2-fenilbenzopiran oz. difenil propanoid (povzeto po Macheix in sod., 1990).
Flavonoidi se dalje delijo v 6 podskupin, ki so poznani pod imenom flavan-3-oli, flavonoli, flavanoli, flavanoni, izoflavoni in antocianini (Moreno in Peinado, 2012). Flavan-3-oli ne obstajajo samo v monomerni obliki (katehin, epikatehin in njuni derivati) ampak tudi kot oligomeri (dimeri, trimeri, tetrameri, idr.) in polimeri (od pet do 100 pa več podenot) teh monomernih flavan-3-olov, ki se imenujejo kondenzirani tanini ali tudi procianidini in prodelfinidini. Slednji so zelo pomembni za kakovost vina, predvsem rdečega (Macheix in sod., 1990, Moreno in Peinado, 2012, Waterhouse in sod., 2016). Flavonoidni fenoli predstavljajo približno 20 % vseh fenolov v belem vinu (Clarke in sod., 2023).
Neflavonoidni fenoli pa se nadalje delijo na fenolne kisline (struktura C6-C1), hidroksicimetne kisline (HCK) (C6-C3) in stilbene (C6-C2-C6) (Macheix in sod., 1990, Moreno in Peinado, 2012, Waterhouse in sod., 2016).
V belem grozdju so glavni fenoli hidroksicimetne kisline – (HCK) – predstavljajo v povprečju skoraj 50 % celokupne vsebnosti fenolov, sledijo monomerni flavan-3-oli ter njihove dimerne in polimerne strukture (kondenzirani tanini) ter flavanoli, kot so kvercetin, miricetin in še stilbeni, med katerimi je najbolj znan resveratrol (Clarke in sod., 2023).
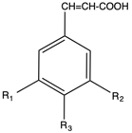
Na sliki 3 se nahajajo glavne vrste hidroksicimetnih kislin grozdja in vina, ki pa v grozdju in vinu obstajajo v zaestreni obliki – največkrat z vinsko kislino (Slika 4).
|
Spojina |
R1 |
R2 |
R3 |
|
cimetna kislina |
H |
H |
H |
|
p-kumarna kislina |
H |
H |
OH |
|
kavna kislina |
H |
OH |
OH |
|
ferulna kislina |
H |
OCH3 |
OH |
|
sinapinska kislina |
OCH3 |
OCH3 |
OH |
Slika 3: Glavne hidroksicimetne kisline grozdja.
Hidroksicimetne kisline (HCK) v grozdju najpogosteje obstajajo kot estri vinske kisline, ki jih poznamo pod imenom kutarna, kaftarna in fertarna kislina. Ker imajo v svoji strukturi dvojno vez, je možna optična rotacija fukcionalnih skupin okrog dvojne vezi, in zato lahko obstajajo v trans– ali cis– konfiguracijah. V naravi je največ trans– oblik HCK. Konfiguracije cis– in trans-lahko tudi zaznamo s kemijsko analizo (kromatografsko te spojine lahko ločimo med seboj), ampak so največkrat prisotne zaradi kemijskih pretvorb v procesu priprave vzorca (Macheix in sod., 1990). Vedno jih je več v kožicah kot v pulpi grozdja. V belem grozdju jih je skupaj nekje okrog 130-150 mg/L (Clarke in sod., 2023), v belih vinih pa je vseh HCK v povprečju 28 mg/L (Rothwell in sod., 2013).
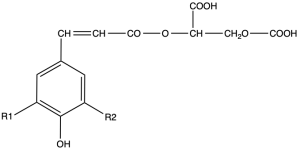
Na sliki 4 se nahaja primer esterske spojine med HCK kislinami in vinsko kislino, in tudi poimenovanja glavnih HCK kislin grozdja in vina, to so kaftarna kislina, kutarna in fertarna kislina. Ko gre grozdje v predelavo, med drozganjem pridejo te fenolne spojine v stik z endogenimi encimi, ki se nahajajo v medceličnini – to so razne hidrolaze (poleg polifenol oksidaz (PPO)), ki tudi cepijo estersko vez, zato je količina esterificiranih HCK v vinu manjša kot je bila v grozdju, najdemo pa v vinu potem tudi nezaestrene HCK, kot so kavna kislina, p-kumarna ali ferulna kislina (Vrhovšek, 1998), ki se lahko pod vplivom encimov kvasovk pretvorijo v hlapne fenole (Moreno in Peinado, 2012, Waterhouse in sod, 2016).
HCK so v začetnih fazah predelave grozdja oksidirane z encimi kot sta lakaza in tirozinaza, kar vodi v porjavenje mošta. Aktivnost teh encimov pa postane manj pomembna s časom, ko oksidacija v vinu postane kemijska. Oksidacija vodi do nastanka temno rjavih odtenkov mošta in vina, in posledično vpliva tudi na zmanjšanje določenih aromatičnih prekurzorjev hlapnih fenolov, reagirajo pa ti produkti kot antioksidanti tudi naprej z drugimi spojinami vina, med njimi tudi s hlapnimi spojinami kot so sortni tioli (Waterhouse in sod., 2016).
|
Cimetna kislina |
R1 |
R2 |
Spojina |
|
p-kumarna kislina |
H |
H |
kutarna kislina |
|
kavna kislina |
OH |
H |
kaftarna kislina |
|
ferulna kislina |
H |
OCH3 |
fertarna kislina |
Slika 4: Kemijska struktura različnih hidroksicimetnih kislin grozdja in vina.
Ferulna in p-kumarna kislina se lahko pod vplivom delovanja encima kvasovk S. cerevisiae cinamat dekarboksilaza pretvorijo v 4-vinil gvajakol in 4-vinil fenol, ki imata C6-C2 strukturo. Največkrat se ju povezuje z vonjavami po klinčkih in zdravilih. Lahko pa ti hlapni fenoli povzročajo tudi neželjene vonjave vin in slabšo kakovost vina. Cinamat dekarboksilaza je endocelularni encim, ki deluje le med alkoholno fermentacijo. Tovrsne encime pa tudi blokirajo ostale fenolne spojine, kar pomeni da je koncentracija vinil fenolov manjša v rdečih vinih (Moreno in Peinado, 2012, Waterhouse in sod., 2016). Več o teh spojinah si lahko preberete v Poglavju 2.
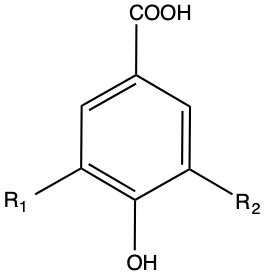
Druga pomembna skupina fenolov belega grozdja in vina so hidroksibenzojske kisline ali fenolne kisline. Hidroksibenzojske kisline so sestavljene iz enega benzenovega obroča in s substitucijo karboksilne kisline (Slika 5) ter hidroksilnimi ali metoksi skupinami na fenolnem obroču. Nahajajo se v vakuolah celic pulpe grozdja in v vakuolah celic kožic. V raztopini voda-etanol so brezbarvne, ko se oksidirajo, pa lahko postanejo temnejše barve (Moreno in Peinado, 2012) .
|
Spojina |
R1 |
R2 |
|
p-hidroksibenzojska kislina |
H |
H |
|
p-protokatehinska kislina |
H |
OH |
|
galna kislina |
OH |
OH |
|
vanilinska kislina |
H |
OCH3 |
|
sinirginska kislina |
OCH3 |
OCH3 |
Slika 5: Glavne hidroksibenzojske kisline grozdja.
Najbolj pogosta hidroksibenzojska kislina v belem vinu je galna kislina (0,32-1,1 mg/100 mL vina), sledijo p-hidroksibenzojska kislina (0,03-0,1 mg/100 ml), p-protokatehinska kislina (0,4-1,2 mg/100 ml), vanilinska kislina (0,04-0,12) in sinirginska kislina (0,007-0,02) (Clarke in sod, 2023).
V raziskavi diplomske naloge polifenolov vin iz grozdja sorte ‘Rebula’ (Vitis vinifera L.) iz Vipavske doline in Goriških brd, pridelanih s podaljšano maceracijo drozge, smo ugotovili, da imajo tovrstna vina izmed posameznih fenolov največ prav galne kisline – od 0,14 pa do 9,2 mg/100 mL (Popova, 2023).
Med neflavonoidnimi fenoli so v belem vinu našli tudi fenolni alkohol tirozol (0,10-0,30 mg/100 mL). Tirozol v vinu nastane iz tirozina med fermentacijo, njegova koncentracija pa je odvisna od seva kvasovk (Gawell in sod., 2018).
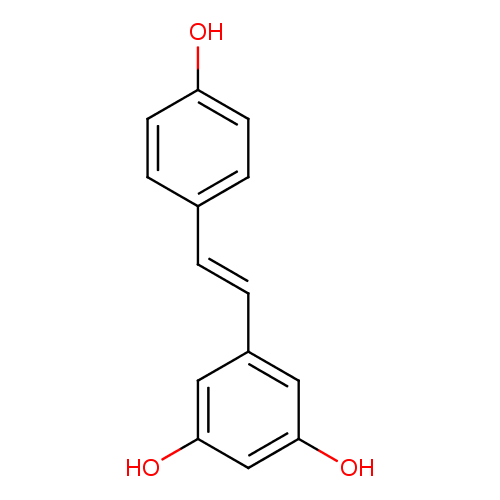
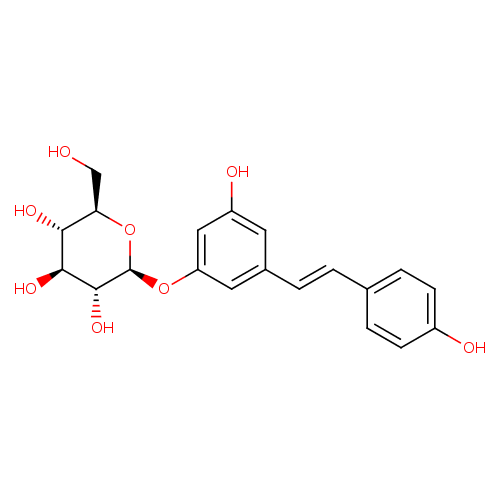
Slika 6 : Glavni stilbeni belega vina; resveratrol (0,03-0,17/100 mL) in resveratrol-3-O-glukozid (0,12-0,61 mg/100mL) (Rothwell in sod., 2013)
Druga skupina fenolov, ki jih je tudi manj v vinih na splošno, so stilbeni, med katerimi je najbolj znan predstavnik trans-resveratrol, ki nastane v grozdju kot odziv rastline na okužbe s patogeni. Derivate resveratrola najdemo le v jagodnih kožicah in v nizkih koncentracijah v belem vinu (~ 0,5 mg/L) (Waterhouse, 2002, Rothwell in sod., 2013), veliko več jih je na primer v vinih iz rdečih sort (~ 3 mg/L) (Rothwell in sod., 2013).
V kemijski strukturi stilbenov gre za dva fenolna obroča, ki ju povezuje veriga etanola ali etilena. Ne prispevajo ne k barvi, ne aromi vina, odlikuje jih močna bioaktivost, s katerimi povezujejo sposobnost pri zadrževanju razvoja bolezni srca in ožilja (Moreno in Peinado, 2012).
V kolikor tehnologija pridelave vin vključuje tudi staranje vina v lesenih sodih, lahko poleg prej omenjenih fenolov, vina vsebujejo tudi hidrolizabilne tanine lesnega izvora. Koncentracija teh spojin v vinih je različna glede na trajanje stika z lesom, poleg drugih dejavnikov, kot sta vrsta lesa ali starost lesa. Vinarji lahko stik z lesom nadomestijo tudi z enološkimi tanini in tovrstni tanini so ponavadi hidrolizabilni.
Hidrolizabilni tanine imenujemo galotanini ali elagotanini. Galotanini nastanejo s polimerizacijo estra galne kisline in D-glukoze. Na Sliki 7 se nahaja struktura estra galne kisline in D-glukoze (Gawell in sod., 2018)
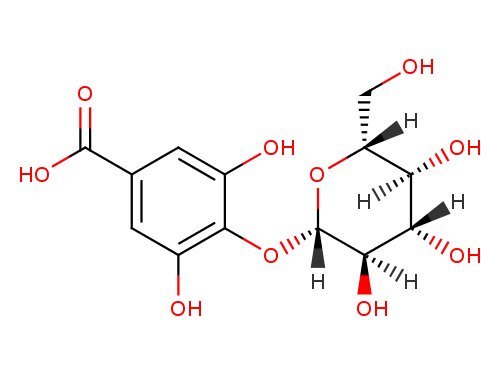
Slika 7: Strukturna formula estra galne kisline in glukoze (Rothwell in sod., 2013)
Elagotanini pa so polimeri elago kisline (Slika 8) – dimera galne ali heksahidroksidifenilne kisline – ki jih pridobivajo iz hrastovega lesa ali pa kostanja (Moreno in Peinado, 2012).
Enološki hidrolizabilni tanini lahko delujejo kot pomembni antioksidanti in antioksidacijska sredstva, ki zmanjšujejo aktivnost oksidacijskih encimov. To kaže na njihov potencialni vpliv na zmanjšanje potrebe po dodajanju SO₂ v procesu pridelave vina. Poleg tega te spojine pomagajo tudi pri obarjanju in bistrenju z bentonitom, vplivajo pa tudi na okus belih vin (Vignault in sod., 2018).
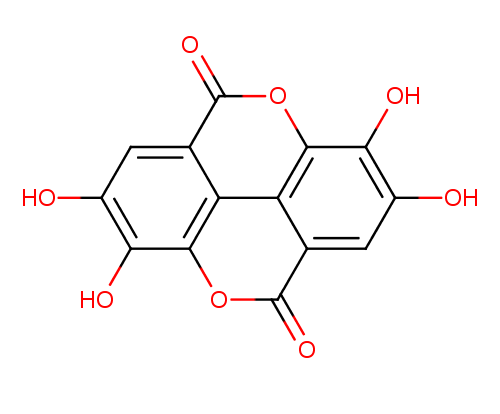
Slika 8: Strukturna formula elago kisline (Rothwell in sod., 2013)
V zadnjih letih nekateri vinarji v pridelavi belih vin uporabljajo tehnike podaljšane maceracije drozge, s kožicami, pulpo in peškami v postopku pridelave vina. Včasih ta vina, zaradi temnejše barve imenujejo tudi “jantarna/amber” vina ali oranžna vina (Milat in sod., 2019). Ta tehnologija vina je zaenkrat še manj raziskana (v primerjavi z rdečimi vini) – pretežno se s tematiko ukvarjajo raziskovalci dežel, kjer tudi vinarji to tehnologijo malce več uporabljajo (npr. Italija, Španija, Hrvaška) (Machado in sod., 2024).
Maceracija drozge belega grozdja zagotovo vpliva tudi na ostale kemijske lastnosti kot so povečanje pH, znižanje celokupne titrabilne kislosti, večjo hlapno kislost, drugačen aromatični profil vin in senzorične lastnosti vin (Darias-Martin in sod., 2020, Sancho-Galan in sod., 2021).
Pomemben vpliv maceracije v pridelavi belih vin pa se kaže v povečani koncentraciji izluženih polifenolov (tudi do 3-krat) in s tem večjo antioksidativno aktivnostjo, grenkobo in trpkostjo in razvojem jantarnih/oražnih odtenkov (Bestulič in sod., 2022). Podaljšana maceracija drozge je priznan postopek v tehnologiji pridelave belih vin, ampak vpliva tega postopka na kakovost in lastnosti vin ne moremo posplošiti, ker je veliko faktorjev, ki lahko vplivajo na kemijske parametre vina (sorta, zrelost, parametri vinifikacije, fermentacije, ipd.).
Na prisotnost polifenolov v belem grozdju in vinu vplivajo različni dejavniki, med drugim sorta grozdja, podnebje, tla, izpostavljenost soncu, trta, grozd in jagoda. Poleg tega ima pri vinu tehnološki postopek ključno vlogo pri spreminjanju količinskega in kakovostnega polifenolnega profila mladega vina, ki se lahko dodatno spremeni z reakcijami med staranjem (Garrido in Borges, 2013, Moreno in Peinado, 2012, Waterhouse in sod., 2026, Clarke in sod., 2023).
S podaljšano maceracijo, predobdelavo z encimi (pektinaze, ß-glukanaze), hladno pred- in med-fermentativno maceracijo v matriks mošta vnašamo zagotovo več polifenolov kot pri tehnologiji pridelave belih vin brez predobdelave kožic z encimi, ali podaljšanega stika mošta s kožicami ali drozgo. Ti fenoli so izpostavljeni različnim reakcijam, ki vplivajo na okus in videz vina, pa tudi na sortne in fermentacijske hlapne spojine (posredno) (Ružič in sod., 2011, Jagatić Korenika in sod., 2018, Garrido-Bañuelos in sod., 2019, Naviglio in sod., 2019, Tomašević in sod., 2019, Sancho-Galan in sod., 2021, Scuturasu in sod., 2021, Bestullić in sod., 2022).
Glavne kemijske reakcije polifenolov belega grozdja med vinifikacijo
Bela vina, kot že prej omenjeno, od polifenolov vsebujejo predvsem hidroksicimetne kisline, ki se v grozdju nahajajo kot estri vinske kisline. Te spojine zelo rade vstopajo v začetne reakcije oksidacije in hidrolize takoj po pecljanju, drozganju in stiskanju. Takrat je prisotnega tudi več kisika in tudi encimi, ki katalizirajo oksidacijo fenolov, so takrat v stiku tudi s spojinami, ki so v grozdju varno shranjene v vakuolah grozdja (npr. fenoli) (Moreno in Peinado, 2012; Vrhovšek, 1997).
V procesu pridelave vina lahko pride do dveh vrst oksidacije:
- encimska,
- ne-encimska.
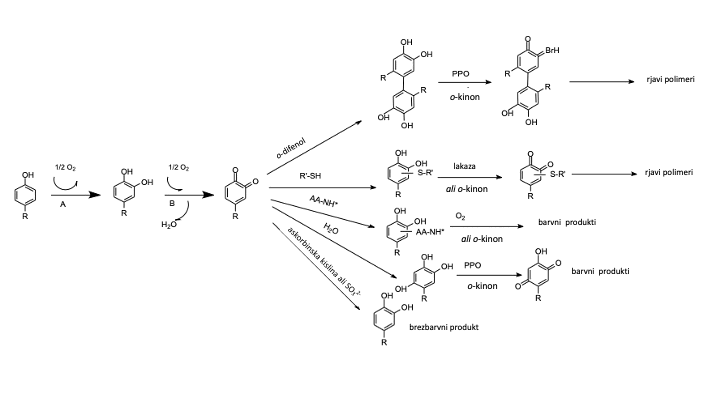
Encimska oksidacija, ki jo katalizirata encima polifenol oksidaza (PPO) in peroksidaza (POD), temelji na vodikovem peroksidu (H2O2) in lahko povzroči porjavelost grozdnega mošta, zlasti zaradi oksidacije HCK kot je kaftarna kislina. Encim PPO začne proces z oksidacijo kaftarne kisline v o-kinone kaftarne kisline (CTAQ), ki s hidroksilacijo, polimerizacijo in kondenzacijskimi reakcijami nadalje reagirajo med seboj in drugimi spojinami in tvorijo rjave pigmente (Li in sod., 2008, Olivera in sod., 2011) (Slika 9).
Kinoni so zelo reaktivni kot oksidanti drugih sestavin mošta, kot so drugi fenoli ali tudi sortni tioli ali estri (Moreno in Peinado, 2012; Waterhouse in sod., 2016). Na tak način nastane tudi acetaldehid, ki nastane s kemijsko oksidacijo etanola. Acetaldehid lahko nadalje reagira tudi s fenolnimi spojinami in sulfiti v vinu, kar nadalje vpliva na svežino in stabilnost vina, ker se na tak način naravna in tudi dodana antioksidativna zaščita vina manjša (Jackson, 2020, Waterhouse in sod., 2016).
Če je encimska oksidacija značilna za začetne faze pridelave vina, je neencimska oksidacija značilna za procese staranja vina.
Neencimska oksidacija v vinu vključuje predvsem oksidacijo polifenolov kot so (+)katehin, (-)-epikatehin, galokatehin, galna kislina in kavna kislina z orto-dihidroksibenzenom (katehol) ali 1,2,3-trihidroksibenzenom (galoil). Ti se pri tem oksidirajo do polikinonskih radikalov in benzokinonov, kisik pa se v tem procesu reducira do vodikovega peroksida ob prisotnosti kovinskih ionov vina Fe3+ in Cu2+, ki se pri tem oksidirajo do Fe2+ oziroma do Cu+. Osrednji del te kemijske oksidacije s pomočjo kovinskih ionov je tako imenovana Fentonova reakcija. Tekom te reakcije iz vodikovega peroksida in železovih ionov nastajajo hidroksilni radikali, ki nadalje oksidirajo organske molekule in spodbujajo njihovo polimerizacijo (Olivera in sod., 2011, Waterhouse in sod., 2016, Zhao in sod., 2023).
Čeprav belo vino ne vsebuje rdečih barvil, lahko ne-encimska oksidacija tudi povzroči spremembe v barvi vina med staranjem. Kinoni, ki nastajajo med oksidacijo, lahko reagirajo z drugimi spojinami in tvorijo rjavkaste pigmente. To povzroči temneješe odtenke belega vina, kar je pogosto znak oksidacije. Pri vinih, ki so bila pridelana s podaljšanim stikom z maceracijo drozge, ki poveča količino fenolov v moštu, in kateri se radi in tudi hitro oksidirajo (zlasti fenoli kot je epikatehin), se ti odtenki pri tovrsnih vinih razvijejo hitreje, ker je fenolov v takšnem vinu več, kot pri vinih, ki niso bila pridelana s procesom podaljšane maceracije drozge (Li in sod., 2008, Zhao in sod., 2023).
Slika 9: Različne reakcije v procesih oksidacije fenolnih spojin.
Sulfiti se običajno dodajajo belemu vinu kot zaščita pred oksidacijo, tudi že v začetnih fazah pridelave vina. Vendar pa lahko kinoni, ki nastanejo med intenzivno encimsko oksidacijo fenolov, reagirajo s sulfiti, kar zmanjša njihovo nadaljno antioksidativno učinkovitost. To pomeni, da je to vino bolj izpostavljeno oksidativnim spremembam v steklenici (Jackson, 2020; Waterhouse in sod., 2016; Riberau-Gayon in sod., 2006). Belo vino tudi nima taninov, ki tudi imajo zaščitno vlogo, kar pomeni, da je to vino bolj občutljivo na oksidacijo kot rdeče vino. Zato je zelo pomembno, da se pri postopkih pridelave belega vina preprečuje prekomerni stikom vina s kisikom, da se ohranita njegova svežina in kvaliteta. K temu lahko pomembno pripomoremo tudi z primerno nizkimi temperaturiami v procesu pridelave belega vina vse od začenih faz pridelave grozdja (Jackson, 2020).
Hlajenje mošta -grozdnega soka pred fermentacijo in tudi med maceracijo je pomembna tehnika, ki vpliva na različne kemijske reakcije, vključno z oksidacijskimi reakcijami fenolnih spojin v belem vinu. Hlajenje mošta lahko znatno zmanjša hitrost oksidacije fenolov, kar je pomembno za ohranjanje svežine, barve in arome belega vina.
Hlajenje mošta upočasni tudi encimske reakcije, vključno z aktivnostjo PPO in lakaze. Nižje temperature zmanjšajo kinetično energijo molekul, zato se reakcije odvijajo počasneje. Posledično je hitrost oksidacije fenolov pri nižjih temperaturah manjša, kar pomaga ohranjati svetlejšo barvo vina (Jackson, 2020).
Poleg encimskih reakcij se fenolne spojine lahko oksidirajo, kot tudi že povedano tudi kemijsko v prisotnosti kisika. Pri hlajenju mošta se topnost kisika v tekočini sicer poveča, vendar nižja temperatura hkrati zmanjša hitrost kemijskih reakcij. To pomeni, da se kljub večji količini raztopljenega kisika oksidacija fenolov upočasni, kar prispeva k ohranjanju polifenolne sestave mošta in preprečevanju nezaželenih barvnih sprememb in sprememb okusa (Ribéreau-Gayon in sod., 2006).
Pred oksidacijo vina pomembno ščiti tudi tripeptid glutation, ki je sestavljen iz aminokislin glicin, cistein in asparaginska kislina. V nekaterih kultivarjih grozdja je naravno prisoten v zelo visokih koncentracijah. Glutation reagira z o-kinoni kaftarne kisline, pri čemer nastane 2-S-glutationil kaftarna kislina, znana kot produkt grozdne reakcije (GRP) (Moreno in Peinado, 2012) in na tak način prepreči oksidacijske reakcije o-kinonov.
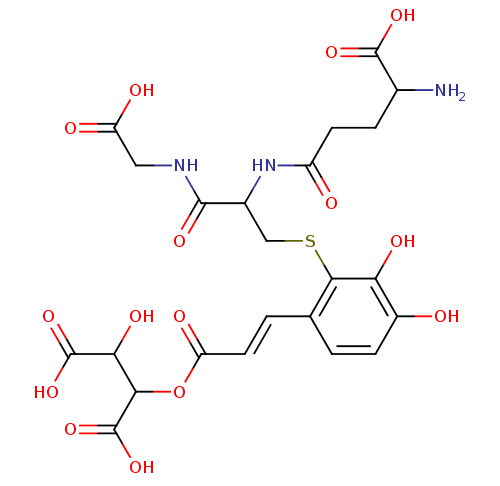
Slika 10: Struktura GRP (Rothwell in sod., 2013)
GRP je brezbarven, ne vstopa v reakcije encimske oksidacije in tako onemogoča nastanek rjavih produktov, saj inaktivira o-kinon kaftarne kisline in zato onemogoča nadaljne reakcije oksidacije. GRP pa se lahko oksidira v prisotnosti prevelike koncentracije kinonov kaftarnih ionov, ki so prisotni v moštu ali vinu takrat, ko se rezerve glutationa izčrpajo, kar povzroči intenzivno porjavelost mošta ali vina. Porjavitev grozdnega mošta je odvisna od relativnega deleža glutationa in hidroksicimetnih kislin (Moreno in Peinado, 2012).
Rjavenje mošta med pred-fermentacijsko obdelavo, kot sta maceracija in hiperoksidacija, lahko učinkovito ustavimo z dodajanjem žveplovega dioksida (SO₂). Dodajanje SO₂ med stiskanjem grozdja ali po njem zmanjša aktivnost PPO in tvorbo o-kinonov kaftarne kisline, in tudi če se kinoni tvorijo, SO₂ pomaga povrniti približno 50 % prvotno prisotne kaftarne kisline in s tem tudi povrnitev v prvotno barvo mošta (Riberau- Gayon in sod., 2006, Moreno in Peinado, 2012).
Bisulfiti (kemijsko aktivna oblika SO2 v raztopini) lahko reducirajo di-kinone v difenole in z vezavo na kinone pobelijo njihovo barvo ter preprečijo nadaljnje oksidativne reakcije. SO₂ tudi reducira vodikov peroksid v vodo, omejuje oksidacijo etanola v acetaldehid ter omejuje oksidacijo askorbinske kisline in o-difenolov (Riberau- Gayon in sod., 2006, Moreno in Peinado, 2012, Jackson, 2020).
Če pa je vsebnost SO₂ v vinu osiromašena, odsotna ali nezadostna, lahko aktivnost PPO in tvorba kinonov povzročita porjavelost tudi brez dodatnega kisika (Vrhovšek, 1997; Moreno in Peinado, 2012). Dodajanje SO₂ med stiskanjem prepreči vezavo kaftarne kisline v GRP, zaradi česar so takšna vina med staranjem bolj nagnjena k porjavelosti (Jackson, 2020).
Grozdje in vina iz belih sort vsebujejo manj polifenolov kot rdeča vina, ki so, tako kot vsi polifenoli, izpostavljena oksidaciji tako v začetnih fazah pridelave vina kot tudi med staranjem vina. Bela vina vsebujejo celokupno precej manj skupnih fenolov kot rdeča vina, ker je v belem grozdju že izvorno manj polifenolov, pa tudi zaradi tega, ker v tehnolgiji pridelavi belih vin velikokrat ni postopka podaljšane maceracije drozge. Pri postopku podaljšane maceracije drozge je potrebno za obogatitev belih vin z večjo kompleksnostjo in antioksidativno zmogljivostjo maceracijo nadzorovati, tako z dolžino kot tudi s temperaturo in nikakor ne smemo pričakovati generalnega/splošnega odziva pri vseh sortah, ker obstajajo razlike tako v sestavi, količini in ekstrabilnosti fenolov iz trdnih delov drozge. Prisotni fenoli belega grozdja so zelo dovzetni za oksidacijo, zlasti v začetni fazi predelave grozdja, kar vodi v nastanek rjavih pigmentov in jantarno barvo takih vin, pa tudi v procesu staranja, če vino ni dovolj zaščiteno z drugimi antioksidanti. Spremembe fenolov med daljšo maceracijo ali staranjem tovrstnih vin še niso dobro poznane. Potrebne so še nadaljnje raziskave za pojasnitev kemijskih reakcij in pretvorb polifenolov belega vina med daljšim stikom s kožicami in staranjem, da bi razvili ciljno usmerjene pristope za proizvodnjo visoko kakovostnih belih vin s podaljšano maceracijo drozge z želenimi senzoričnimi in zdravju koristnimi lastnostmi.
Viri
Arapitsas, P., Oliveira, J., & Mattivi, F. (2015). Do white grapes really exist? Food Research International, 69, 21–25. https://doi.org/10.1016/j.foodres.2014.12.002
Bestulić, E., Rossi, S., Plavša, T., Horvat, I., Lukić, I., Bubola, M., Ilak Peršurić, A. S., Jeromel, A., & Radeka, S. (2022). Comparison of different maceration and non-maceration treatments for enhancement of phenolic composition, colour intensity, and taste attributes of Malvazija istarska (Vitis vinifera L.) white wines. Journal of Food Composition and Analysis, 109. https://doi.org/10.1016/j.jfca.2022.104472
Clarke, S., Bosman, G., du Toit, W., & Aleixandre-Tudo, J. L. (2023). White wine phenolics: Current methods of analysis. Journal of the Science of Food and Agriculture, 103(1), 7–25. https://doi.org/10.1002/jsfa.12120
Darias-Martı́n, J. J., Rodrı́guez, O., Dı́az, E., & Lamuela-Raventós, R. M. (2000). Effect of skin contact on the antioxidant phenolics in white wine. Food Chemistry, 71(4), 483–487. https://doi.org/10.1016/S0308-8146(00)00177-1
Dos Santos, J. R. M., & Kempka, A. P. (2025). White wine vinification and an expanded insight into pellicular macerations: Bibliometric and bibliographic review. Journal of the Science of Food and Agriculture, 105(1), 19–41. https://doi.org/10.1002/jsfa.13685
Garrido-Bañuelos, G., Buica, A., Schückel, J., Zietsman, A. J. J., Willats, W. G. T., Moore, J. P., & Du Toit, W. J. (2019). Investigating the relationship between cell wall polysaccharide composition and the extractability of grape phenolic compounds into Shiraz wines. Part II: Extractability during fermentation into wines made from grapes of different ripeness levels. Food Chemistry, 278, 26–35. https://doi.org/10.1016/j.foodchem.2018.10.136
Gutiérrez-Escobar, R., Aliaño-González, M. J., & Cantos-Villar, E. (2021). Wine Polyphenol Content and Its Influence on Wine Quality and Properties: A Review. Molecules, 26(3), 718. https://doi.org/10.3390/molecules26030718
Jackson, R. S. (2020). Wine science: Principles and applications (Fifth Edition). Academic Press.
Jagatić Korenika, A. M., Maslov, L., Jakobović, S., Palčić, I., & Jeromel, A. (2018). Comparative study of aromatic and polyphenolic profiles of Croatian white wines produced by cold maceration. Czech Journal of Food Sciences, 36(6), 459–469. https://doi.org/10.17221/448/2017-CJFS
Li, H., Guo, A., & Wang, H. (2008). Mechanisms of oxidative browning of wine. Food Chemistry, 108(1), 1–13. https://doi.org/10.1016/j.foodchem.2007.10.065
Lucarini, M., Durazzo, A., Lombardi-Boccia, G., Souto, E. B., Cecchini, F., & Santini, A. (2021). Wine Polyphenols and Health: Quantitative Research Literature Analysis. Applied Sciences, 11(11), 4762. https://doi.org/10.3390/app11114762
Macheix, J.-J., Fleuriet, A., & Billot, J. (2018). Fruit phenolics (Reissued). CRC Press.
Moreno, J., & Peinado, R. (2012). Enological chemistry (1st ed). Academic Press.
Naviglio, D., Formato, A., Scaglione, G., Montesano, D., Pellegrino, A., Villecco, F., & Gallo, M. (2018). Study of the grape cryo-maceration process at different temperatures. Foods, 7(7). https://doi.org/10.3390/foods7070107
Oliveira, C. M., Ferreira, A. C. S., De Freitas, V., & Silva, A. M. S. (2011). Oxidation mechanisms occurring in wines. Food Research International, 44(5), 1115–1126. https://doi.org/10.1016/j.foodres.2011.03.050
Pascual, O., Vignault, A., Gombau, J., Navarro, M., Gómez-Alonso, S., García-Romero, E., Canals, J. M., Hermosín-Gutíerrez, I., Teissedre, P.-L., & Zamora, F. (2017). Oxygen consumption rates by different oenological tannins in a model wine solution. Food Chemistry, 234, 26–32. https://doi.org/10.1016/j.foodchem.2017.04.148
Ribéreau‐Gayon, P., Glories, Y., Maujean, A., & Dubourdieu, D. (2006). Handbook of Enology: The Chemistry of Wine Stabilization and Treatments (1st ed.). Wiley. https://doi.org/10.1002/0470010398
Rothwell, J. A., Perez-Jimenez, J., Neveu, V., Medina-Remón, A., M’Hiri, N., García-Lobato, P., Manach, C., Knox, C., Eisner, R., Wishart, D. S., & Scalbert, A. (2013). Phenol-Explorer 3.0: A major update of the Phenol-Explorer database to incorporate data on the effects of food processing on polyphenol content. Database, 2013, bat070. https://doi.org/10.1093/database/bat070
Ružić, I., Škerget, M., Knez, Ž., & Runje, M. (2011). Phenolic content and antioxidant potential of macerated white wines. European Food Research and Technology, 233(3), 465–472. https://doi.org/10.1007/s00217-011-1535-4
Sancho-Galán, P., Amores-Arrocha, A., Jiménez-Cantizano, A., & Palacios, V. (2021). Influence of the Presence of Grape Skins during White Wine Alcoholic Fermentation. Agronomy, 11(3), 452. https://doi.org/10.3390/agronomy11030452
Scutarașu, E.-C., Luchian, C. E., Vlase, L., Colibaba, L. C., Gheldiu, A. M., & Cotea, V. V. (2021). Evolution of phenolic profile of white wines treated with enzymes. Food Chemistry, 340, 127910. https://doi.org/10.1016/j.foodchem.2020.127910
Tomašević, M., Lisjak, K., Vanzo, A., Česnik, H. B., Gracin, L., Ćurko, N., & Ganić, K. K. (2019). Changes in the composition of aroma and phenolic compounds induced by different enological practices of Croatian white wine. Polish Journal of Food and Nutrition Sciences, 69(4), 343–358. https://doi.org/10.31883/pjfns/112328
Vignault, A., González-Centeno, M. R., Pascual, O., Gombau, J., Jourdes, M., Moine, V., Iturmendi, N., Canals, J. M., Zamora, F., & Teissedre, P.-L. (2018). Chemical characterization, antioxidant properties and oxygen consumption rate of 36 commercial oenological tannins in a model wine solution. Food Chemistry, 268, 210–219. https://doi.org/10.1016/j.foodchem.2018.06.031
Vrhovšek, U. (1998). Extraction of hydroxycinnamoyltartaric acids from berries of different grape varieties.Journal of agricultural and food chemistry,46(10), 4203–4208.
Waterhouse, A. L., Sacks, G. L., & Jeffery, D. W. (2016). Understanding Wine Chemistry. In Understanding Wine Chemistry. https://doi.org/10.1002/9781118730720
Zhao, X., Duan, C.-Q., Li, S.-Y., Zhang, X.-K., Zhai, H.-Y., He, F., & Zhao, Y.-P. (2023). Non-enzymatic browning of wine induced by monomeric flavan-3-ols: A review. Food Chemistry, 425, 136420. https://doi.org/10.1016/j.foodchem.2023.136420