2 Sestava vinske arome
Diana Alexandra Martin Rojas, Melita Sternad Lemut in Guillaume Antalick
Center za raziskave vina, Fakulteta za vinogradništvo in vinarstvo, Univerza v Novi Gorici, Glavni trg 8, Vipava
diana.martin@ung.si
Uvod
S kemijskega vidika je vino kompleksna matrica, sestavljena iz ogromnega števila različnih hlapnih in nehlapnih spojin, ki lahko vzbudijo zaznave različnih odtenkov vonja in arome [1](Sáenz-Navajas in sod., 2012). Njegova kompleksnost je odvisna od sorte, geografskega porekla, lastnosti vinograda, vinogradniških tehnik ter postopkov vinifikacije in zorenja (Marín-San Román in sod., 2020; Ruiz in sod., 2019; Sáenz-Navajas in sod., 2012). Vonj je ena od značilnosti, ki pomembno odraža kakovost vina, njegovo izražanje pa je povezano s hlapnimi organskimi spojinami (v nadaljevanju mednarodno uveljavljena kratica VOC (volatile organic compounds)). V vinu je bilo do danes identificiranih več sto takšnih spojin; med njimi so kemijske družine, kot so terpeni, pirazini, tioli, laktoni, višji alkoholi in estri, pa tudi druge vrste molekul, med njimi npr. hlapni fenoli.
Uvodoma je pomembno opozoriti, da se slovenska in tuja literatura ter praksa razlikujeta v razumevanju terminov vonj in aroma. Razliko med njima opredeljuje tudi v slovenski jezik preveden standard ISO 5492:2008 »Senzorična analiza – Slovar«. V njem je vonj definiran kot organoleptična lastnost, zaznavna z vohalnim organom med vdihavanjem hlapnih snovi. Aroma pa se zaznava šele, ko vino vlijemo v ustno votlino, kjer se zaradi višje telesne temperature hitro ogreje, kar poveča hlapnost aromatičnih spojin, dodatno pa jo pospeši mešanje tekočine z jezikom. Aromatične spojine torej soustvarjajo tako vonj kot aromo vina. V nadaljevanju besedila bomo zaradi terminološke poenostavitve uporabljali izraz vonj, razen kadar bo potrebno razlikovanje ali v primeru ustaljene terminologije.
Človek je sposoben zaznave velikega števila VOC v zelo majhnih koncentracijah. VOC zaznavamo z vohalnim sistemom bodisi ortonazalno (skozi nos)[2] bodisi retronazalno (skozi usta)[3] s pomočjo specifičnih celičnih receptorjev. Da jih je mogoče zaznati, pa morajo spojine posedovati določene lastnosti kot so visok parni tlak, delna topnost v vodi, lipofilnost in nizka molekulska masa (Genovese in sod., 2009). Prav tako morajo biti prisotne vsaj v najmanjši koncentraciji, pri kateri jih je še mogoče zaznati. Ta raven, imenovana prag zaznave[4], je odvisna od vinske matrice ter se lahko močno razlikuje med posameznimi spojinami. Razmerje med koncentracijo in vrednostjo praga zaznave se imenuje vrednost aktivnosti vonja (Odour Activity Value – OAV) in se pogosto uporablja kot pokazatelj aromatičnega potenciala hlapnih spojin. Čeprav je ta pristop ustrezen pri enostavnih matricah, je njegova uporabnost pri kompleksnih matricah, kot je vino, omejena zaradi pomembnih kemičnih in senzoričnih interakcij, opisanih v nadaljevanju. Po drugi strani pa vse hlapne spojine ne prispevajo enako k aromatični sestavi vina, niti niso prisotne v enakih koncentracijah. Tako lahko nekatere spojine, prisotne v vinu le v sledovih (ng/L ali celo pg/L), prispevajo več kot druge v območju mg/L (Ribéreau-Gayon in sod., 2017). Zaznavanje vonja sicer še ni povsem pojasnjeno. Analize VOC v vinu so pokazale, da so aromatične spojine in njihovi predhodniki (v uporabi je tudi izraz prekurzorji) skupni vsem sortam grozdja, vendar se njihove koncentracije in razmerja med njimi v vinih razlikujejo, kar povzroča različne zaznave v različnih posameznih vinih (Atanasova in sod., 2005). Poleg tega se je izkazalo, da lahko tudi nekatere nehlapne spojine medsebojno učinkujejo in vplivajo na zaznavo vonja (Sáenz-Navajas in sod., 2010). Prav tako lahko nekateri sinergijski učinki med VOC vplivajo na značilnosti celotne matrice (Ruiz in sod., 2019). V kompleksni matrici, kot je vino, pa lahko tudi nekatere spojine, čeprav prisotne pod njihovim pragom zaznave, vseeno prispevajo k celokupnemu aromatičnemu profilu vina (Atanasova in sod., 2005). Splošno gledano lahko številne oblike kemičnih in senzoričnih interakcij povzročajo kvalitativne senzorične zaznave, povezane z velikimi aromatičnimi razlikami med vini (Atanasova in sod., 2005; Ruiz in sod., 2019).
Klasifikacija aromatičnih spojin v vinu je odvisna od njihovega izvora oziroma od tega, kdaj se te spojine tvorijo pred/med vinifikacijskim procesom. Tako lahko aromatične spojine opredelimo kot sortne ali primarne arome, če nastanejo že v grozdju. Fermentacijske ali sekundarne arome so spojine, ki se običajno tvorijo s pomočjo delovanja encimov mikroorganizmov, predvsem vinskih kvasovk (Saccharomyces cerevisiae) med alkoholno fermentacijo (v nadaljevanju AF) in nekaterih mlečnokislinskih bakterij. Zorilne arome ali terciarne arome pa nastajajo po fermentaciji, tekom zorenja oz. staranja vina. Sproščanje in/ali biosinteza novih spojin povzroča spremembe vonja med vinifikacijo. Tudi po končani vinifikaciji, med zorjenjem in staranjem vina, lahko potekajo različne vrste reakcij. Zato vonj vina ni nekaj statičnega, temveč se lahko razvija skozi čas, pri čemer je njegova zaznava s strani potrošnikov odvisna od sestave vinske matrice. Naslednje poglavje bo podrobneje obravnavalo nastanek in klasifikacijo spojin, povezanih z vonjem in aromo vina.
Primarne arome
Primarne oziroma sortne arome so povezane s spojinami, ki jih najdemo v grozdju in so lahko prisotne v prosti ali vezani obliki kot njihovi predhodniki, ki so brez vonja (Ribéreau-Gayon in sod., 2017; Ruiz in sod., 2019). Ti nehlapni predhodniki se lahko med vinifikacijskim procesom spremenijo v hlapno obliko bodisi na račun delovanja mikroorganizmov (kvasovk, mlečnokislinskih bakterij) bodisi preko kemičnih reakcij, ki jih omogoča vinski medij – glej Poglavje 8 (Moreno-Arribas in Polo, 2009). Včasih so primarne arome povezane s kakovostjo vina oz. senzorično tipiko vina, saj lahko izražajo edinstvenost posamezne sorte. Takšni primeri so cvetlične note pri sorti muškat, vonj paprike pri nekaterih sortah, kot je npr. cabernet sauvignon, ali vonj popra pri sorti shiraz (Ribéreau-Gayon in sod., 2017). Skupina primarnih arom vključuje različne kemične družine, med katerimi so npr. metoksipirazini, tioli, terpeni in norizoprenoidi.
Metoksipirazini
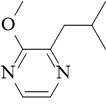
Nekatera vina opisujemo z izrazom (deskriptorjem) “rastlinsko”, kar je pogosto povezano s prisotnostjo metoksipirazinov (v nadaljevanju MP) (Ruiz in sod., 2019). MP so dušikovi heterocikli, ki nastajajo preko metabolizma aminokislin. Rastline biosintetizirajo MP, da zaščitijo dozorevajoče sadje (grozdje) pred zaužitjem s strani plenilcev. Vsebnost MP v vinih je odvisna od sorte, podnebja ter lastnosti vinograda in vinogradniških praks (tla, klon, koreninska podlaga, upravljanje z listno steno vinske trte). Prisotni so predvsem v vinih, pridelanih iz grozdja t.i. “bordojskih sort”, kot so sauvignon, cabernet franc, cabernet sauvignon, merlot in še nekaj drugih. Te spojine so močni povzročitelji vonjav z zelo nizkimi pragovi zaznave (Tabela 1). V vinih je najbolj zastopan 3–izobutil–2–metoksipirazin (IBMP) (1–30 ng/L). Vonj te spojine opisujemo kot vonj po zeleni papriki in grahu (Ribéreau-Gayon in sod., 2017; Ruiz in sod., 2019). IBMP se tvori v grozdnih jagodah med zeleno fazo, njegova koncentracija pa se od fenološke faze véraison dalje zmanjšuje (Bindon in sod., 2014; Roujou De Boubée in sod., 2000). Običajno so MP prisotni v grozdju in vinih v razponu koncentracij okoli 2–30 ng/L (Lei in sod., 2018). Pri nekaterih sortah, kot je na primer cabernet sauvignon, lahko prisotnost teh spojin prispeva h kompleksnosti. Vendar pa se na splošno obravnavajo kot negativne za kakovost vina, zlasti pri rdečih vinih (Ruiz in sod., 2019) in so v prevelikih koncentracijah nezaželene pri potrošnikih.
Tioli
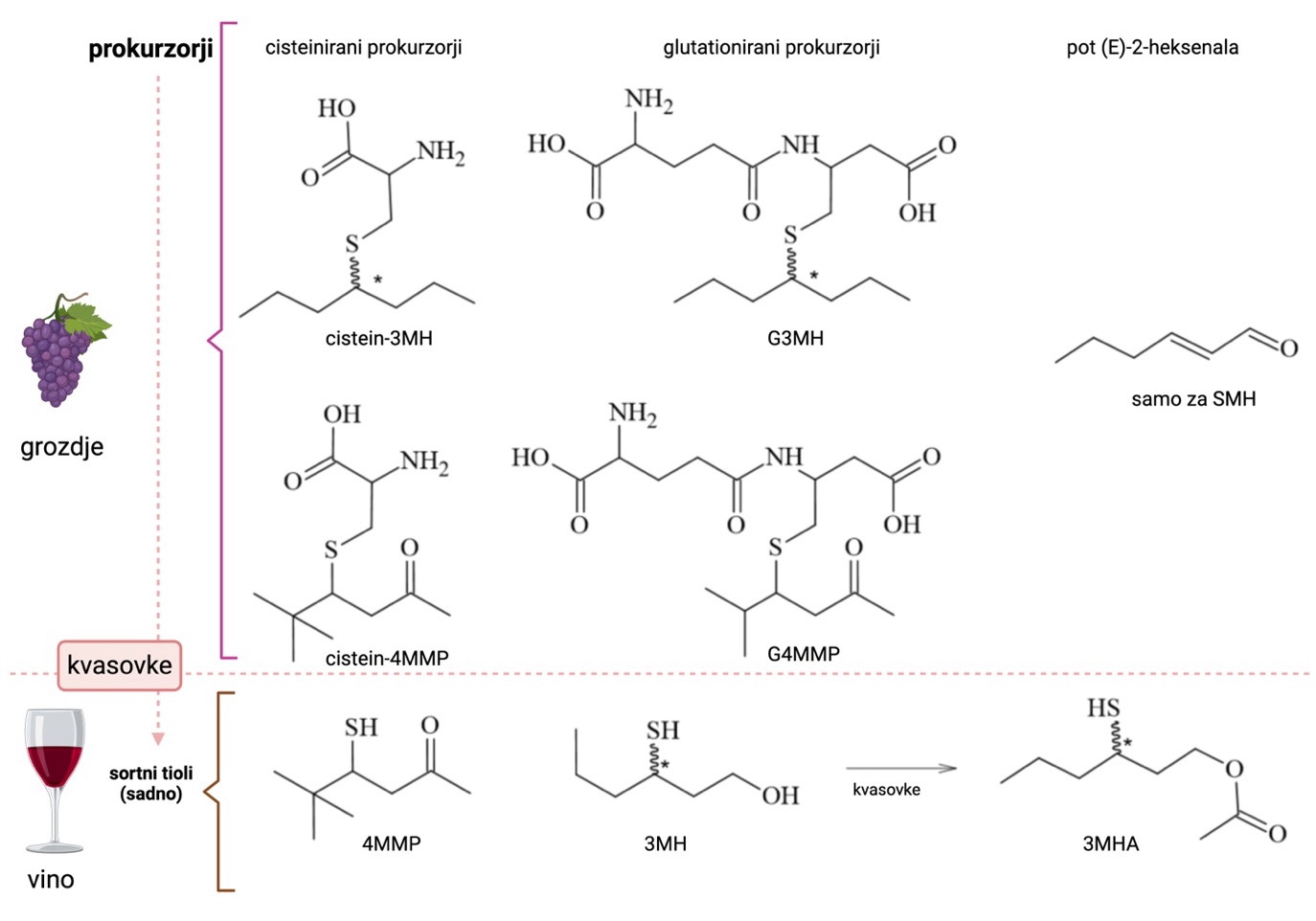
Spojine s tiolno funkcionalno skupino (-SH), imenujemo s skupnim imenom tioli in so običajno povezane z napakami v vinu. Vendar pa lahko tioli, ki izhajajo iz grozdja, predstavljajo redke pozitivne izjeme, saj so ključni za aromatično sestavo, ki določa note tropskih sadežev, kot so pasijonka, grenivka in guava. Tovrstne vonjave so zaznavne v nekaterih belih in rose vinih in so dobro sprejete med potrošniki (Iobbi in sod., 2023; King in sod., 2011). Tioli se lahko v grozdju pojavljajo kot nearomatični, nehlapni predhodniki, ki jih lahko kvasovke sprostijo med fermentacijo na račun aktivnosti encimov β-liaz (Ruiz in sod., 2019). Najpogosteje so prisotni kot S-konjugati s cisteinom. Poleg tega se pojavljajo tudi v drugih oblikah, kot so glutationski konjugati ali vezave s tripeptidi (Glu-Cys-Gly) ter dipeptidi (Cys-Gly oziroma Glu-Cys) (Slika 1) (Ribéreau-Gayon in sod., 2017; Roland in sod., 2011. Ti predhodniki izhajajo v grozdja, njihova koncentracija pa je večja v kožicah kot v mesu grozdne jagode. Po drugi strani pa se vsebnosti in vrste teh spojin razlikujejo glede na sorto. Na primer, vsebnosti so večje pri sortah, kot je sauvignon (Roland in sod., 2011).
Tako v rdečih kot belih vinih je bilo do danes identificiranih in kvantificiranih več različnih tiolov. Gre za molekule z močnim prispevkom k vonju vina. Med vsemi identificiranimi molekulami so bili nekateri tioli, kot so 4-merkapto-4-metil-2-pentanon (4MMP), 3-merkaptoheksil acetat (3MHA) in 3-merkapto-1-heksanol (3MH), prepoznani kot molekule v ozadju močnih sortnih značajev. Posebej pomembni so za aromatično tipičnost vin, pridelanih iz grozdja sorte sauvignon, lahko pa prispevajo tudi k sortni aromi vin iz drugih sort in specifičnih regij (Schlich in sod., 2015). V francoskih in novozelandskih vinih iz grodja sorte sauvignon se koncentracije gibljejo od 4 do 40 ng/L za 4MMP, od 26 do 18.000 ng/L za 3MH ter do 2.500 ng/L za 3MHA. Te vrednosti so precej nad pragom zaznave (Tabela 1). Na vsebnost in ohranitev tiolov med vinifikacijskim procesom lahko vplivajo različni dejavniki, kot so ustrezna izbira kvasovke, višja fermentacijska temperatura, ki lahko poveča njihove koncentracije, ter dodatek SO₂, ki pomaga pri njihovem ohranjanju skozi čas (Coetzee in du Toit, 2012).
Terpenoidi
Pri muškatnih sortah so terpenoidi prisotni v mesu in kožici grozdnih jagod tako v prosti obliki kot vezani na sladkorje (glikozidi), običajno na disaharide (Ribereau-Gayon in sod., 1975). Pri drugih sortah so terpenoidi večinoma prisotni (kot glikozidi) v jagodni kožici. V grozdju in vinu se nahaja širok spekter terpenoidov, ki pa vsi izvirajo iz t. i. poti mevalonske kisline (Slika 2).Glede na število ogljikovih atomov jih delimo na monoterpenoide (10 C), seskviterpenoide (15 C), di-terpenoide (20 C) in tri-terpenoide (30 C) (Goodwin, 1964; Ruiz in sod., 2019). Monoterpenoidi v vinu vključujejo ogljikovodike, aldehide, alkohole, kisline in estre (Ribéreau-Gayon in sod., 2017). V vinih je bilo do danes identificiranih približno 50 različnih aromatičnih spojin, ki izhajajo iz skupine monoterpenoidov, večina pa pomembno prispeva k citrusnim in cvetličnim senzoričnim zaznavam (Black in sod., 2015). Monoterpenoidi se lahko uporabijo tudi za identifikacijo nekaterih sort. Muškatne sorte na primer izstopajo s svojim prepoznavnim in izrazitim vonjem zaradi bistveno večjih koncentracij monoterpenoidov v primerjavi z drugimi sortami (Linsenmeier in sod., 2022; Ribéreau-Gayon in sod., 2017). Med njimi so v velikih koncentracijah, okoli 5 ppm, prisotni linalool, geraniol, citral, citronelol, nerol in α-terpineol. Po drugi strani pa lahko terpenoidi pomembno prispevajo tudi k vonju drugih, ne-muškatnih sort, kot sta npr. renski rizling in dišeči traminec (Ruiz in sod., 2019). Najbolj značilni monoterpenoidi v vinih so linalol, (E)-hotrienol, citronelol, geraniol, nerol, (–)-cis-rose oksid in α-terpineol, ki jih povezujemo predvsem s cvetličnimi, sadnimi in začimbnimi notami.
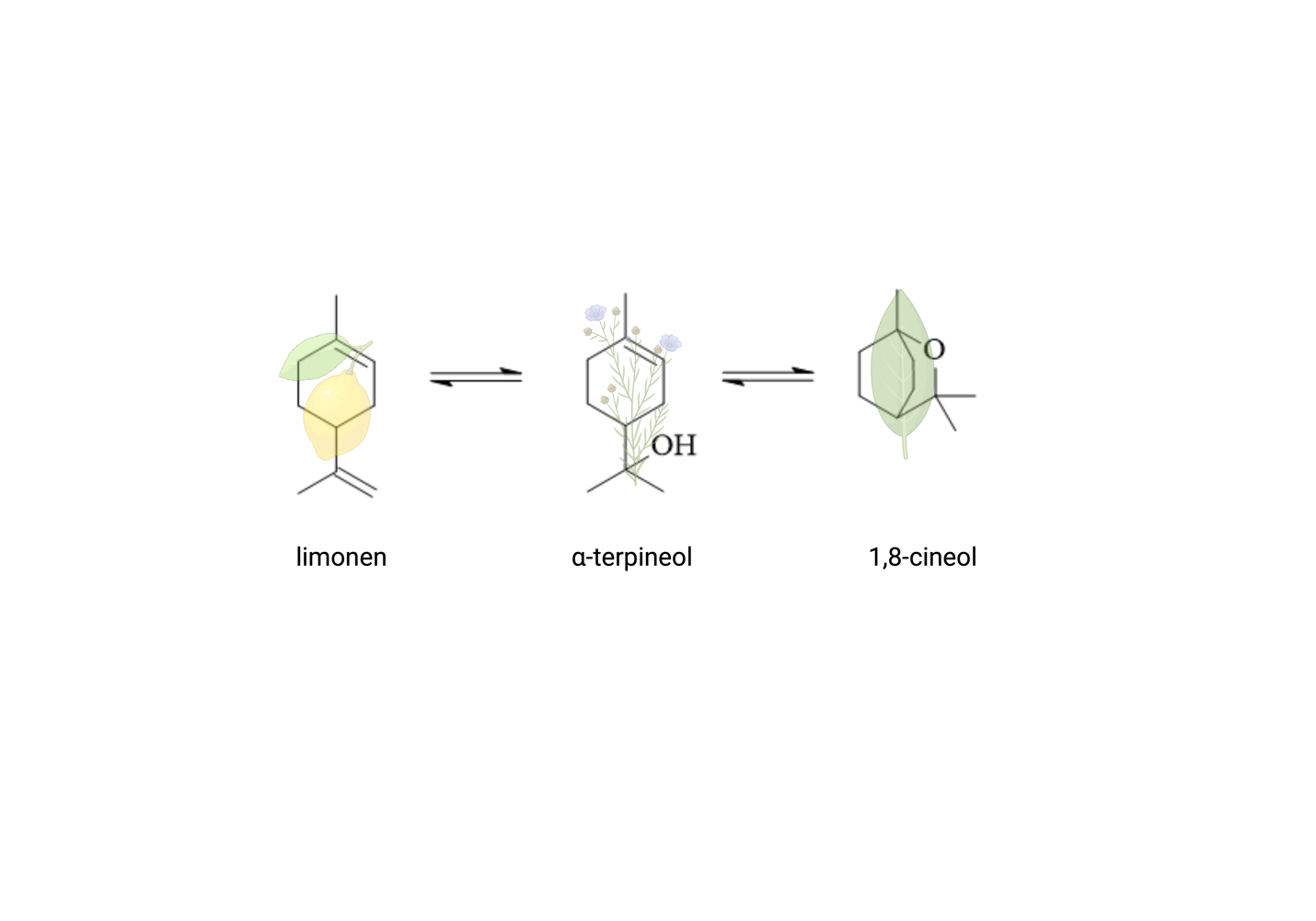
Pomembnost terpenoidov je potrjena tudi v aromatični sestavi rdečih vin. Kot kaže, lahko spojine, kot so 1,8-cineol, 1,4-cineol in drugi derivati p-mentana, prispevajo k svežim notam mete (mint), črnega ribeza, sena in suhih zelišč, tudi če so prisotne v majhnih koncentracijah (Antalick in sod., 2015; Fariña in sod., 2005; Poitou in sod., 2017; Slaghenaufi in sod., 2022). V različnih rdečih vinih pa je bil identificiran tudi seskviterpen rotundon, ki je povezan z začimbnimi deskriptorji, kot je “črni poper”.
Koncentracije terpenoidov v vinu so odvisne od številnih dejavnikov, med drugim od tipa tal, podnebnih razmer in vinogradniških praks; pri ne-muškatnih sortah se vrednosti gibljejo v razponu od ng/L do µg/L (Black in sod., 2015; Carrau in sod., 2008; Yuan in sod., 2015). Med vinifikacijo pa se vsebnosti lahko spreminjajo glede na sev kvasovk, pH vrednost medija, dolžino trajanja maceracije ter temperature po trgatvi in med zorenjem, kar lahko privede bodisi do povečanja bodisi do zmanjšanja koncentracij teh spojin – več o tem v Poglavju 8 (Carrau in sod., 2008; Hjelmeland in Ebeler, 2015; Yuan in sod., 2015). Med zorenjem oz. staranjem vina so terpenoidi podvrženi različnim kemičnim transformacijam, kot so izomerizacija, zapiranje obroča (ciklizacija), hidratacija, dehidratacija in oksidacija (Cheynier in sod., 2010). Aromatična spojina (aglikon) se iz svoje glikozidne oblike sprošča bodisi z encimsko bodisi s kemično hidrolizo. Med AF in jabolčno-mlečnokislinsko fermentacijo (MLAF) se nekatere od teh spojin sproščajo s pomočjo β-glukozidaz, ki jih proizvajajo mikroorganizmi (Ruiz in sod., 2019). Po drugi strani pa so med staranjem vina zaznali kislinsko hidrolizo, pri kateri se terpenoidi lahko preuredijo in tvorijo nove aromatične spojine (Slika 3) (Black in sod., 2015; Carrau in sod., 2008; Fariña in sod., 2005).
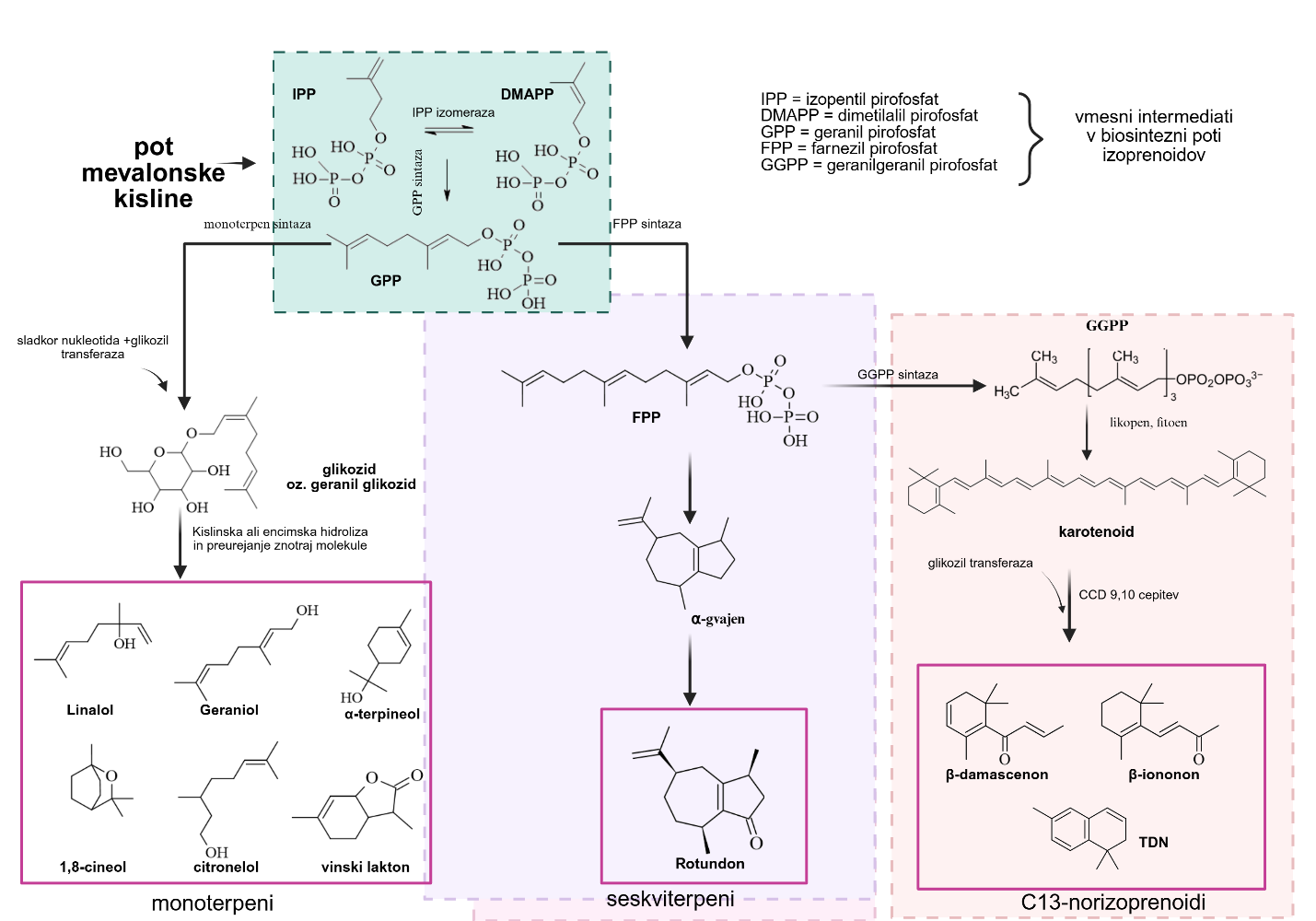
Norizoprenoidi
Tako kot terpenoidi so tudi norizoprenoidi pomembni za številne aromatične profile vin, saj lahko prispevajo različne note, od cvetličnih in sadnih do petrolejskih (Black in sod., 2015). Njihove koncentracije v vinih se gibljejo v razponu ng/L in µg/L. Nastajajo kot produkti biološke razgradnje karotenoidov (Slika 2). Norizoprenoidi lahko vsebujejo 9, 10, 11 ali 13 ogljikovih atomov, pri čemer so v grozdju najpogostejši C13-norizoprenoidi (Ribéreau-Gayon in sod., 2017). V grozdju so njihovi nehlapni predhodniki prisotni v velikih koncentracijah kot glikozidi, njihova pretvorba v končne aromatično aktivne spojine pa naj bi potekala med procesom vinifikacije in staranjem v steklenici in sicer preko kislinsko katalizirane reakcije (Black in sod., 2015).
Po začetku zorenja grozdja (post-véraison) začne koncentracija karotenoidov upadati na račun tvorbe C13-podenot, ki se nato glikozilirajo. V grozdju so koncentracije nehlapnih predhodnikov ali glikozidov C13-norizoprenoidov višje kot koncentracije prostih hlapnih spojin (Black in sod., 2015; Mendes-Pinto, 2009). Kvasovkine β-glukozidazne encimske aktivnosti jih pomagajo iz predhodnikov sprostiti med vinifikacijo, medtem ko jih kisla hidroliza med in po alkoholni fermentaciji običajno preuredi v aromatične norizoprenoide. Znano je, da abiotski dejavniki, kot so svetloba, temperatura in voda, vplivajo na koncentracije C13-norizoprenoidov. Vinogradniške prakse, kot je odstranjevanje listov, lahko vplivajo na povečano tvorbo norizoprenoidov (Bubola in sod., 2020; Palai in sod., 2023; Zhu in sod., 2022).
Najpogostejši C13-norizoprenoidi v vinih so β-damascenon ter α- in β-iononi. α- in β-iononi so bolj povezani s cvetličnimi deskriptorji (npr. vijolice) kot β-damascenon (note kuhane jabolke in medu) (Ferreira in sod., 2000). Poleg tega nekateri izoprenoidi izkazujejo sinergijske učinke z drugimi vrstami spojin, kar tudi lahko vpliva na zaznavanje vonja. Prisotnost β-damascenona, tudi v majhnih koncentracijah, lahko v kombinaciji z drugimi spojinami okrepi sadni vonj jagodičevja (Escudero in sod., 2007; Pineau in sod., 2007). V to družino spada tudi TDN (1,1,6-trimetil-1,2-dihidronaftalen), ki ga običajno opisujemo kot vonj po kerozinu ali petroleju. Ta spojina prispeva predvsem k vonju renskega rizlinga, čeprav je prisotna tudi v nekaterih drugih belih in rdečih sortah. Njena koncentracija se med staranjem povečuje (Black in sod., 2015).
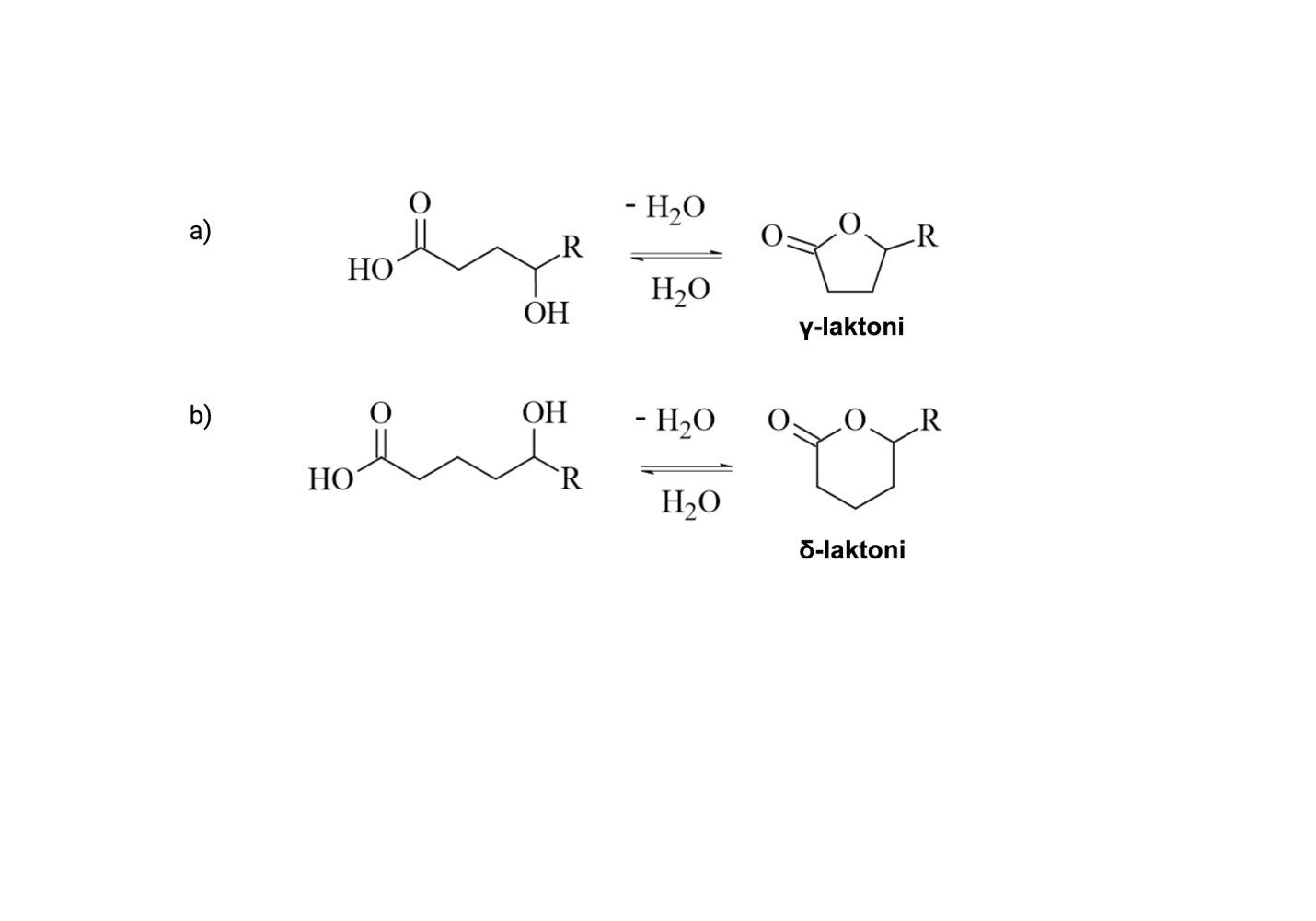
Laktoni
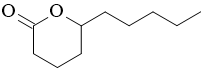
Laktoni so spojine, ki nastanejo z esterifikacijo, pri čemer sta funkcionalna karboksilna skupina in alkoholna skupina za reakcijo prisotni v isti molekuli. Ta skupina zajema številne nasičene 5-členske (γ) in 6-členske (δ) laktone z enostavnimi alkilnimi substituenti (Slika 4). Nekateri laktoni, prisotni v vinih, izhajajo iz hrastovih sodov (trans-whiskey lakton, kokos) in fermentacije (butirolakton, maslo/karamela). Po drugi strani pa so laktoni, ki izhajajo iz grozdja, povezani s sadnimi zaznavami, kot so breskev, marelica, kokos, suho sadje, in z začimbno-zelenimi, ter z vonjem po maščobah in olju (Allamy in sod., 2018a). Koncentracije laktonov v vinu se gibljejo v razponu µg/L, pogosto pa so večje v rdečih kot v belih vinih (Miller in sod., 2022). V vinih so bili do danes identificirani in kvantificirani različni predstavniki te skupine, med njimi γ-nonalakton, δ– in γ-dekalakton, 2-nonen-4olid, masoia lakton in nekateri p-mentanski laktoni, znani tudi kot vinski lakton, ki prispevajo k aromatičnemu profilu (Ferron in sod., 2020). Običajno jih najdemo v večjih koncentracijah v vinih iz dehidriranega grozdja (izsušene jagode) (Allamy in sod., 2018a; Šuklje in sod., 2016).
V ozadju tvorbe laktonov naj bi po predvidevanjih sodelovali različni predhodniki, med drugim 4-oksnonanska kislina pri nastanku γ-nonalaktona (Ferron in sod., 2020), masoia lakton pri nastanku δ-dekalaktona (Pons in sod., 2017) ter ustrezne 4-hidroksikarboksilne kisline pri nastanku drugih linearnih alifatskih laktonov (Slika 4) (Miller in sod., 2022). Eden najpomembnejših predstavnikov je γ-nonalakton, ki spominja na kompleksno mešanico kokosa, breskve in kuhanega sadja. Čeprav je njegova koncentracija v vinu običajno manjša od njegovega praga zaznave, lahko prisotnost tega laktona skupaj z drugimi laktoni prispeva k vonju vina zaradi sinergijskih učinkov, hkrati pa lahko okrepi učinek drugih spojin in prispeva k notam suhega sadja, kot so slive in fige, ki jih najdemo v nekaterih vinih sorte merlot (Allamy in sod., 2018a).
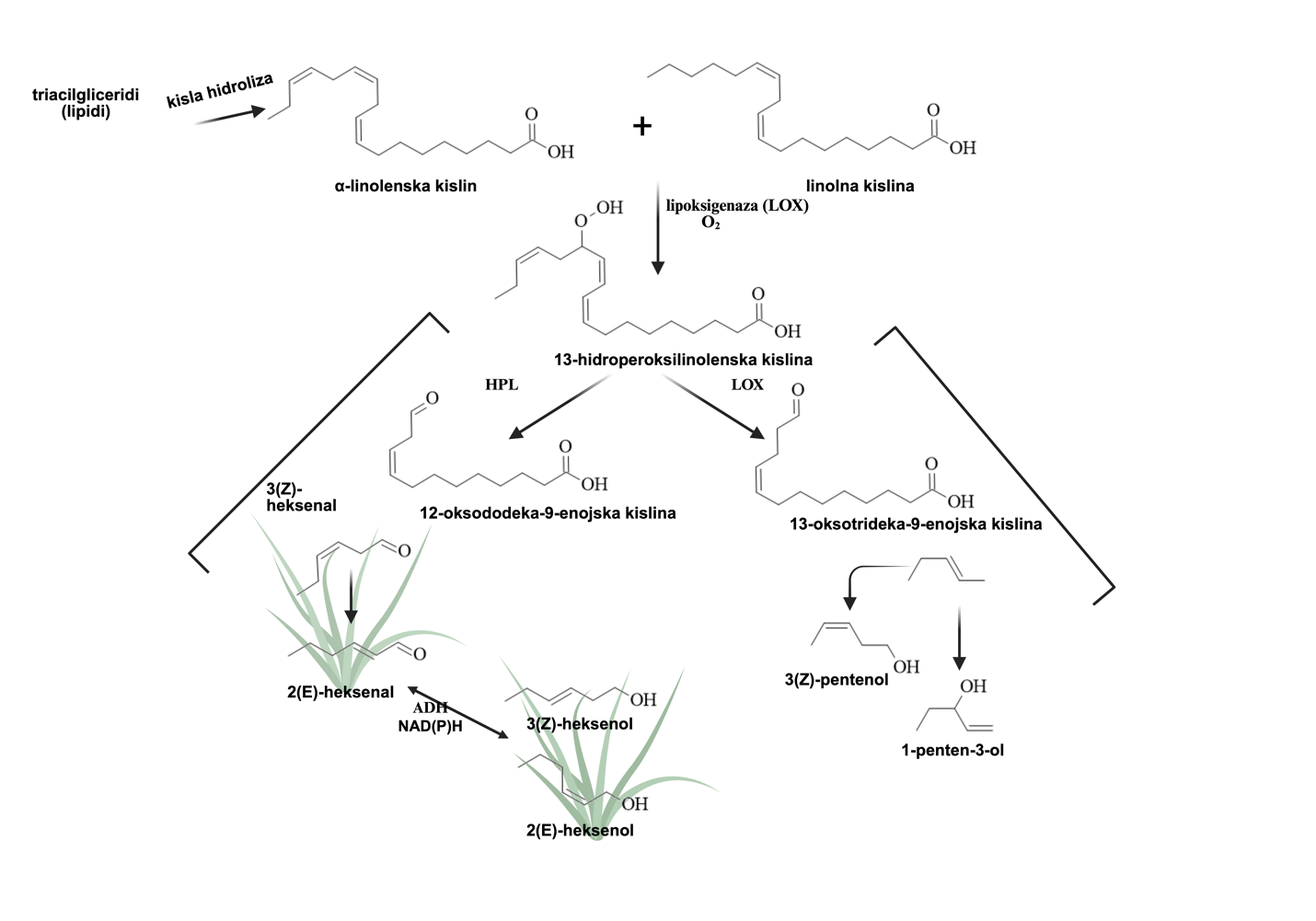
Spojine s šestimi ogljikovimi atomi
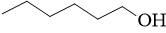
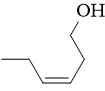
Alkoholi in aldehidi s šestimi ogljikovimi atomi (C6) so hlapne spojine, ki lahko prispevajo k zeliščnim senzoričnim zaznavam vina. Nastanejo z oksidacijo maščobnih kislin (ang. fatty acids (FA)) preko lipoksigenazne (LOX) poti (Slika 5) npr. tekom drozganja grozdnih jagod (Mozzon in sod., 2016). Nekateri C6 karbonilni derivati so povezani z zeleno-sadnimi notami, medtem ko so nekateri C9 karbonili odgovorni za kumarične in melonine note (Salas in sod., 2013). C6-aldehidi so pomembne hlapne spojine v moštu, a se kasneje med AF večinoma reducirajo v C6-alkohole.
Koncentracija C6 spojin se giblje od nekaj µg/L do mg/L in je odvisna od sorte in zrelosti grozdja. Opisno jih definiramo kot vonj po pokošeni travi. Pogosteje identificirani C6-alkoholi v vinih so 1-heksanol, (Z)-3-heksenol in (E)-2-heksenol; med aldehidi pa 1-heksanal in (E)-2-heksenal (Mozzon in sod., 2016).
Furanoni
Karamela in kuhana jagoda sta deskriptorja, ki sta pogosto povezana s prisotnostjo Furaneola® (4-hidroksi-2,5-dimetil-3(2H)-furanona) in homofuraneola (2-etil-4-hidroksi-5-metil-3(2H)-furanona) v vinu. To je pogosto opisano predvsem pri ne-Vitis vinifera vinih, kjer se lahko koncentracije povzpnejo tudi do 1 mg/L. Tudi pri Vitis vinifera vinih so bile te spojine identificirane in kvantificirane nad pragom zaznave (furaneol 49 μg/L in homofuraneol 26,5 μg/L) (Ribéreau-Gayon in sod., 2017). Poleg tega so lahko koncentracije teh spojin večje v vinih iz grozdja poznih trgatev (Allamy in sod., 2018b) in v vinih iz grozdja okuženega z Botrytis cinerea (Sarrazin in sod., 2007). Furanoni izhajajo iz grozdja, vendar natančnejši mehanizmi njihove tvorbe v grozdju in vinu še niso pojasnjeni. Čeprav so koncentracije teh spojin večje pri vinih iz grozdja ameriških vrst trte kot evropskih, se domneva, da ima njihova prisotnost v slednjih sinergijski vpliv na sadno zaznavo (Ferreira in sod., 2002; Sasaki in sod., 2015).
Sekundarne arome
Med alkoholno fermentacijo kvasovke tvorijo pomembne aromatične spojine, kot so višji alkoholi, maščobne kisline in estri.
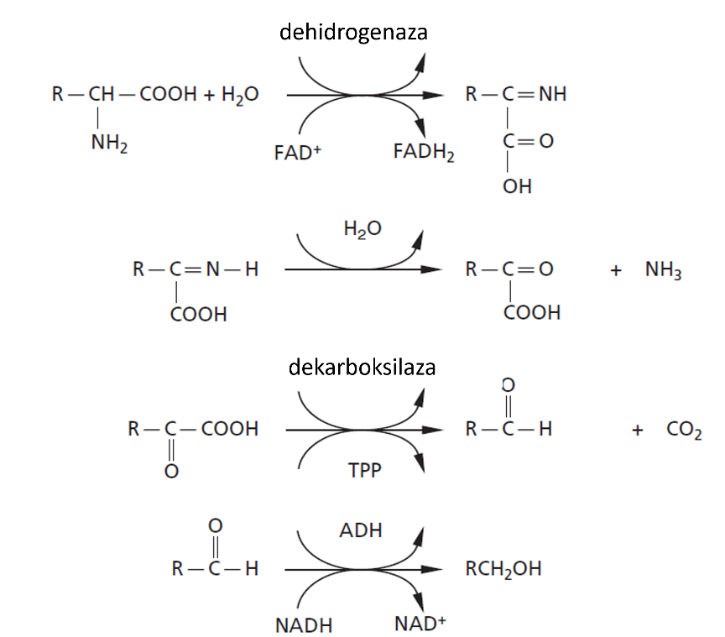
Višji alkoholi
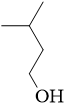
Višji alkoholi so alkoholi z več kot dvema ogljikovima atomoma v verigi. Njihove koncentracije se gibljejo od 0,2 do 1,2 g/L v belih vinih in od 0,4 do 1,4 g/L v rdečih vinih (Ribéreau-Gayon in sod., 2017). Te spojine pomembno prispevajo k aromatični kompleksnosti vin. Pri koncentracijah pod 300 mg/L lahko prispevajo k izrazitejšim zaznavam sadnih in cvetličnih not, medtem ko lahko koncentracije nad 400 mg/L zakrijejo nekatere lastnosti vina in povzročijo pojav ostrih in neprijetnih not (de-la-Fuente-Blanco in sod., 2016a; Etievant, 1991; Rapp in Mandery 1986). Te molekule kvasovke sintetizirajo iz sladkorjev in nekaterih aminokislin (Slika 6), nastale koncentracije pa so spremenljive in odvisne od seva kvasovk (Ribéreau-Gayon in sod., 2017).
Višji alkoholi kot skupina pomembno prispevajo k aromatičnemu ozadju vseh fermentiranih pijač. Poleg tega so substrati za nastanek acetatnih estrov višjih alkoholov, ki se običajno opisujejo kot spojine s pomembnim prispevkom k sadnemu značaju vin .
Pri tvorbi višjih alkoholov (na račun delovanja kvasovk) je ključna vsebnost dušika v moštu (Cordente in sod., 2021). Poleg tega lahko temperatura fermentacije, pH, raztopljeni kisik, motnost mošta in prisotnost prehodnih kovin prav tako vplivajo na količino teh spojin – glej Poglavje 8 (Muñoz in sod., 2006; Pires in sod., 2014). Običajno so višji alkoholi prisotni v večjih koncentracijah v rdečih vinih.
Hlapne kisline
Približno 10–15 % celokupne vsebnosti kislin v vinih predstavljajo hlapne kisline, pri čemer največ prispeva ocetna kislina, ki je glavni vir hlapne kislosti vina. Hlapne kisline pomembno modulirajo aromatične značilnosti vina, vendar koncentracije ocetne kisline nad pragom zaznave (0,7 g/L) povzročajo vonj po kisu in lahko poslabšajo kakovost vina. Njihova vsebnost je zato regulirana z zakonodajo. Večje koncentracije ocetne kisline lahko kažejo na delovanje določenih ne-saccharomyces kvasovk pred fermentacijo ali pa nastanejo kasneje zaradi delovanja mlečnokislinskih ali ocetnokislinskih bakterij (Ribéreau-Gayon in sod., 2017). V odvisnosti od stila vina se za optimalne lahko smatrajo vsebnosti med 0,2–0,7 g/L.
Maščobne kisline s srednje dolgo verigo
V fermentiranih pijačah maščobne kisline s srednje dolgo verigo (MCFA) predstavljajo karboksilne kisline z verigami, dolgimi od štirih do dvanajst ogljikovih atomov. Kvasovke tvorijo te kisline med biosintezo lipidov kot vmesne produkte, ki se nato vgrajujejo v njihove lipidne membrane. V skladu s poročanji delujejo te spojine kot pomembni regulatorji stresa, hkrati pa so lahko toksične za kvasne celice in imajo inhibitorni učinek tudi na mlečnokislinske bakterije (Lambrechts in Pretorius, 2000). To pojasnjuje kasnejšo esterifikacijo dela teh spojin. Po drugi strani pa se razvejane kisline lahko tvorijo iz aminokislin preko iste poti kot višji alkoholi (Slika 6). Najpomembnejše razvejane kisline so izobutanojska kislina, izovalerjanska kislina in 2-metilbutanojska kislina. Posamezno spominjajo na vonj po siru in znoju, vendar lahko v vinski matrici prispevajo k aromatični kompleksnosti in so predhodniki nekaterih najbolj aromatičnih estrov v vinih.
Estri
Tvorba estrov je rezultat reverzibilne reakcije med alkoholi in organskimi kislinami (Slika 7). V vinu je širok spekter alkoholov in kislin, kar omogoča nastanek različnih vrst estrov. Ti se lahko tvorijo tako encimsko (z encimi katalizirane reakcije) med AF, kot tudi kemično, glede na ravnotežje substratov med staranjem vina (Ribéreau-Gayon in sod., 2017). Na splošno lahko njihove koncentracije dosežejo velikost reda mg/L, vendar je njihova tvorba močno odvisna od seva kvasovke. S to skupino spojin je običajno povezan sadni značaj vina (Cameleyre in sod., 2015; Falcao in sod., 2012; Lytra in sod., 2016; Ribéreau-Gayon in sod., 2017).
Aromatične estre lahko razdelimo v tri skupine: etilni estri maščobnih kislin (EEFA); acetati višjih alkoholov (HAA), in etilni estri razvejanih kislin (Cheynier in sod., 2010; Ribéreau-Gayon in sod., 2017). Na splošno tvorba estrov temelji na sevu kvasovke, sestavi grozdnega mošta in tehnoloških odločitvah v vinifikacijskem procesu (Lambrechts in Pretorius, 2000).
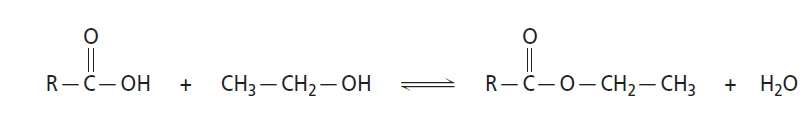
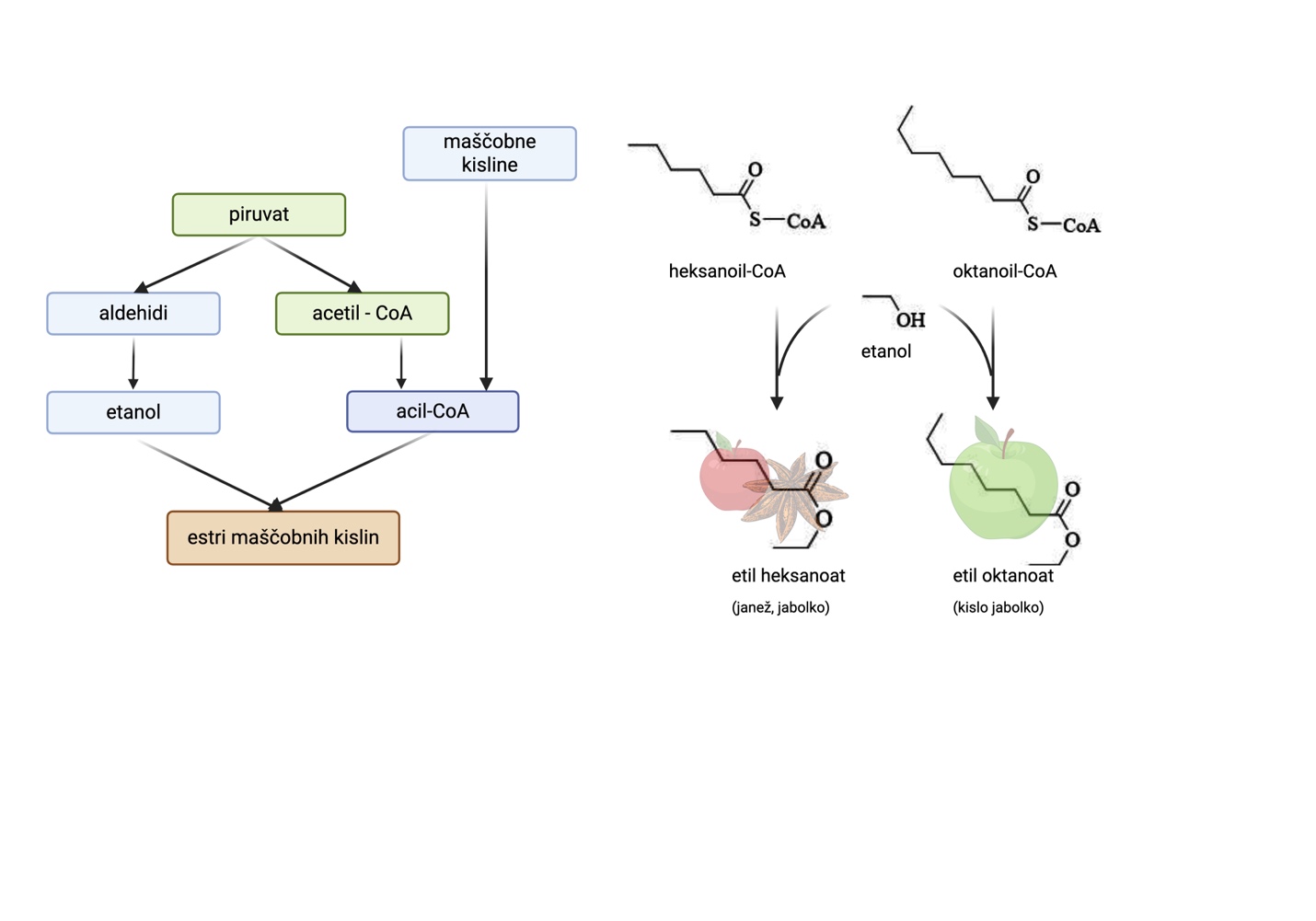
Etilni estri maščobnih kislin
Etilni estri maščobnih kislin (EEFA) prispevajo k sadnim vonjem vina in vključujejo predstavnike kot so: etil butirat (zrela jagoda, kivi), etil heksanoat (jagoda, ananas), etil oktanoat (kislo jabolko) in etil dekanoat (jabolčna lupina, cvetlične note) (Aznar in Arroyo, 2007). Na splošno se te spojine smatra kot pomemben prispevek k vonju mladih belih vin. Sintetizirajo se preko encimskih reakcij med AF, pri čemer kvasovke izkoriščajo etanol in maščobne kisline s srednje dolgo verigo (Slika 8) (Ribéreau-Gayon in sod., 2006; Xue in sod., 2022). Modulacija EEFA je povezana z različnimi dejavniki. Poročali so, da je dodajanje predhodnikov MCFA v fermentacijski medij povzročilo povečano tvorbo etilnih estrov (Saerens in sod., 2008). Nižja temperatura fermentacije pa po poročanjih vodi do večjih vsebnosti MCFA in pripadajočih EEFA (Kong in sod., 2021; Saerens in sod., 2008).
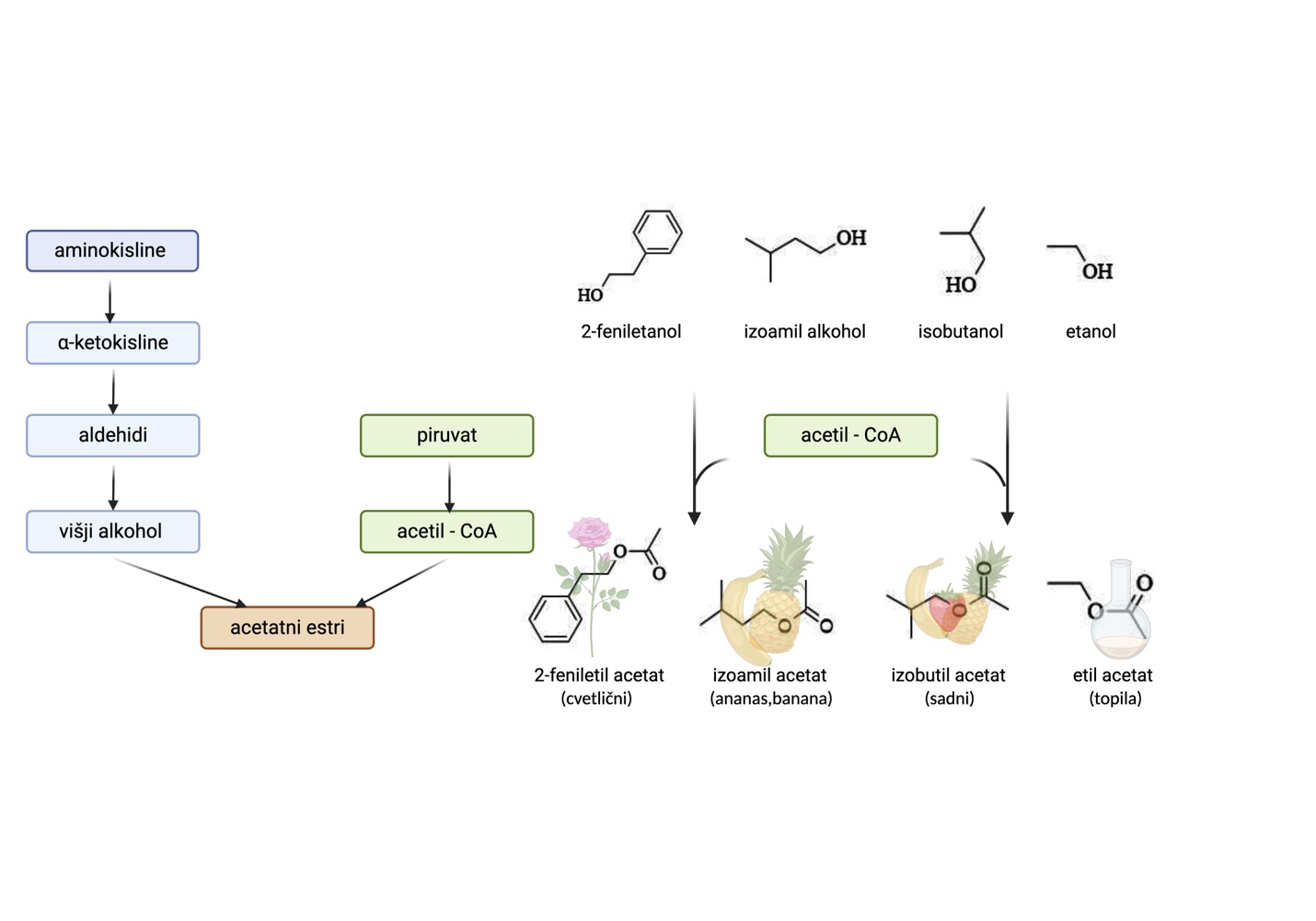
Acetatni estri višjih alkoholov
Acetatni estri višjih alkoholov (HAAs) se tvorijo s pomočjo encimov iz acetil-CoA (predhodnik ocetne kisline) in višjega alkohola (Slika 9). HAAs so še posebej podvrženi hidrolizi tekom let staranja belega vina (Antalick in sod., 2014). Prispevajo k aromatični kompleksnosti, vendar imajo hkrati velik aromatični potencial in lahko zakrijejo sortni značaj vina (Ribéreau-Gayon in sod., 2006).
Etil acetat je eden najpomembnejših estrov v vinu s kvantitativnega vidika. Med fermentacijo ga kvasovke tvorijo v zmernih količinah, med staranjem v lesenih sodih pa lahko razvoj ocetnokislinskih bakterij povzroči nastanek velikih količin skupaj z ocetno kislino. Odgovoren je za pojav “acescence”, to je zadušljiv vonj po kisu. Prag zaznav te spojine je 200-krat nižji kot pri ocetni kislini. Kadar je koncentracija nad 150 mg/L, lahko poslabša aromatično sestavo vina (Amerine in Cruess, 1960), medtem ko lahko manjše količine, pod 120 mg/L, prispevajo k aromatični kompleksnosti (Ribéreau-Gayon in sod., 2006).
Izоamil acetat je ena najpomembnejših spojin med HAAs in ima vonj po banani. Njegova koncentracija v vinu lahko doseže do 6 mg/L (Aznar in Arroyo, 2007), običajno pa je prisoten v količinah nad pragom zaznave (Tabela 1). Podobno je heksil acetat povezan z vonji po hruški in nekaterimi drugimi descriptorji, kot so zeliščne, sadne in grozdne note (Sumby in sod., 2010). Pogosto te spojine v grozdnem moštu še niso prisotne, saj nastanejo kot produkt AF. Sev kvasovk in sestava grozdnega mošta (dušik, lipidi) sta glavna dejavnika, ki vplivata na pojavnost HAAs, pri čemer ima sestava grozdja večji vpliv na njihov nastanek v primerjavi z EEFA (Antalick in sod., 2015).
Estri razvejanih kislin
Ti estri nastanejo z reakcijo razvejanih kislin z etanolom, predvsem med staranjem vina (Díaz-Maroto in sod., 2005). Glavni predstavniki te skupine vključujejo: etil izobutirat, etil 2-metilbutirat, etil izovalerijat s sadnimi notami ter etil fenilacetat z descriptorji po vrtnici, medu in tobaku (Ribéreau-Gayon in sod., 2017). Posamezno spadajo med najbolj aromatične estrske spojine v vinu. Dokazano je, da prispevajo k vonju po temnem sadju in so še posebej pomembni za vonj rdečih vin (de-la-Fuente-Blanco in sod., 2016b; Lytra in sod., 2013). Njihova vsebnost v vinu je neposredno povezana s prisotnostjo pripadajočih razvejanih kislin. Zato so sestava grozdja, sev kvasovk in pogoji fermentacije ključni dejavniki, ki določajo vsebnost EEBA v vinu. Večje koncentracije so bolj običajne v rdečih vinih, zlasti po nekaj letih staranja (Antalick in sod., 2014).
Druge fermentacijske spojine
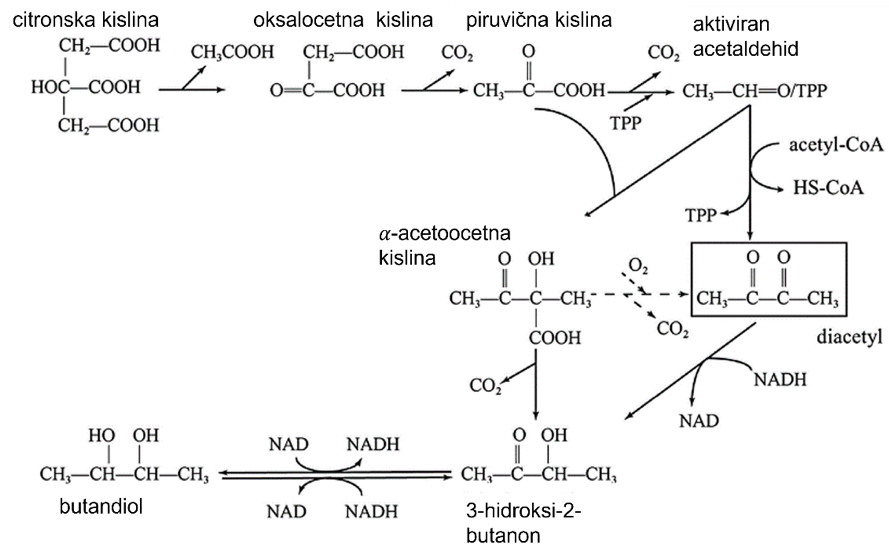
Diacetil
Kvasovke med AF proizvedejo le majhne količine diacetila (butan-2,3-dion), glavnina pa nastane med jabolčno-mlečnokislinsko fermentacijo (Slika 10). Mlečnokislinske bakterije sintetizirajo spojine kot je diacetil iz citronske kisline ali drugih karbonilnih spojin, pri čemer produkti pomembno prispevajo k značilnim mlečnim oziroma maslenim notam. Ta vrsta spojin lahko prispeva h kompleksnosti terciarne arome, saj so zelo reaktivne in lahko reagirajo z drugimi spojinami ter tvorijo tiazole in heterociklične spojine z vonjem po kavi in lešnikih (Marchand in sod., 2000, 2011).
Terciarne arome
Zorenje oz. staranje vina se nanaša na razvoj kemijske sestave vina po fermentaciji. Poteka lahko v sodih, posodah iz nerjavečega jekla ali celo neposredno v steklenici – v vseh primerih pa se arome s časom spreminjajo.
V predhodnih razdelkih tega poglavja smo že obravnavali nastanek spojin različnega izvora (sortnega in fermentacijskega), ki lahko prispevajo k kemičnim reakcijam med zorenjem vina, kar vodi v nastanek terciarne arome vina, imenovane tudi cvetica (bouquet).
Ena najpomembnejših terciarnih spojin, ki prispeva k cvetici, je dimetil sulfid (DMS). DMS spominja na vonj konzervirane koruze in rakovih palčk, vendar lahko v vinski matrici prispeva note tartufov in temnega sadja. Posebej pomemben je pri izražanju značilne cvetice rdečih vin, pridelanih iz »bordojskih« sort (Picard in sod., 2015). DMS nastaja pretežno med zorenjem vina preko hidrolize S-metilmetionina (Segurel in sod., 2005). Njegov prag zaznave so določili pri 25 μg/L, pri čemer so v vinih zaznane koncentracije med 11 in 760 μg/L (Siebert in sod., 2010).
Terciarna aroma lahko izvira tudi iz stika vina z lesenim (najpogosteje hrastovim) sodom med zorenjem – glej Poglavje 8. Spojine, kot so hrastovi laktoni, furanove spojine, derivati vanilina in fenolni derivati, lahko prehajajo iz soda v vino (Castro-Vázquez in sod., 2011). Na sestavo hrastovega lesa, uporabljenega v pridelavi sodov, in s tem na potencial ekstrakcije v vino pomembno vplivajo različni dejavniki, kot so botanična vrsta hrasta, rastišče (poreklo), prostornina in oblika soda (razmerje med notranjo površino soda in volumnom vina, ki je z njo v stiku). Pomembna je tudi starost sodov, saj se dinamika ekstrakcije spojin z leti uporabe spreminja (Pérez-Prieto in sod., 2002). V Evropi se za sode največ uporabljata vrsti hrasta Quercus robur in Q. petraea, v ZDA pa Q. alba (Chatonnet in sod., 1999). Glede aromatičnih spojin ameriški hrast praviloma prispeva več trans-viski (whiskey) laktona, ki daje intenzivno noto kokosa. Razlike so opazne tudi v koncentraciji C13-norisoprenoidnih spojin (Ortega-Heras in sod., 2004; Sefton in sod., 1990).
Iz hrasta je bilo doslej ekstrahiranih in identificiranih več kot 200 hlapnih spojin (Ortega-Heras in sod., 2004), pri čemer so vrste in koncentracije teh spojin v veliki meri odvisne od stopnje žganja lesa med obdelavo (Courregelongue in Pons, 2024). Stopnja žganja hrasta (temperatura, trajanje) vpliva na nastanek aromatičnih spojin zaradi razgradnje (termolize) lesnih polimerov – lignina, celuloze in hemiceluloze – ter Maillardovih reakcij (Castro-Vázquez in sod., 2011; Sefton in sod., 1990; Ortega-Heras in sod., 2004; Qian in sod., 2022). Med njimi so pomembni hlapni fenoli, kot sta gvajakol in 4-metilgvajakol, ki nastaneta iz lignina med segrevanjem hrastovih sodov in v vino vnašata značilne dimne note (Ortega-Heras in sod., 2004; Qian in sod., 2022). Proces zorenja v sodu je tudi na splošno povezan s povečanjem števila in koncentracije hlapnih fenolov, pri čemer variacije izvirajo tako iz različne vsebnosti hidroksicimetnih kislin v grozdju kot tudi iz že omenjenih lastnosti lesa ter trajanja stika med vinom in lesom (Qian in sod., 2022). Nastanek hlapnih fenolov je lahko odvisen tudi od prisotnosti kvarnih mikroorganizmov, kot je Brettanomyces bruxellensis; v takšnih primerih visoke koncentracije teh spojin povzročijo note, ki se štejejo za napako in negativno vplivajo na kakovost vina (Ribéreau-Gayon in sod., 2017). Rdeča vina, ki zorijo v lesenih sodih, so ob neustreznem nadzoru procesa zorenja posebej občutljiva na kontaminacijo s kvasovko Brettanomyces; nastanejo lahko visoke koncentracije 4-etilfenola in 4-etilgvajakola, ki vinu dajejo značilne živalske, hlevske in usnjene note (Chatonnet in sod., 1993, 1994). Vanilin, ki prav tako izvira iz lignina, je eden glavnih derivatov hrastovih sodov in pogosto presega prag zaznave (400 µg/L v belem vinu in 320 µg/L v rdečem vinu) (Spillman in sod., 2004). Iz pentoz, osnovnih komponent hemiceluloze, se lahko tvori furfural, ki prispeva note mandljev. Nadaljnja reakcija furfurala z vodikovim sulfidom vodi do nastanka furfuriltiola, odgovornega za vonj po popečenem kruhu in kavi, pogosti zaznavi v vinih, zorjenih v novih sodih.
Tabela 1. Naslednja tabela povzema glavne družine spojin, povezanih s sestavo arome vina.
|
Družina |
Ime |
Zgradba |
Vonj, opisno[5] |
Prag zaznave[6] |
Koncentracija |
|
|
Pirazini |
2-metoksi-3-izobutilpirazin (IBMP) |
|
zelena paprika |
1 ng/L 16 ng/L[7] |
2-56 ng/L[8] |
|
|
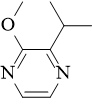
3-izopropil-2-metoksipirazin (IPMP)
|
|
grah (sladkast), šparglji |
40 ng/L[9] |
1-10 ng/L[10] |
||
|
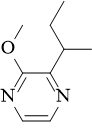
3-sec-butil-2-metoksipirazin (SBMP) |
|
zeleni grah, po zatohlem, paprika |
2-5 ng/L[11] |
2-16 ng/L[12] |
||
|
Tioli |
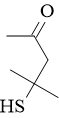
4-merkapto-4-metil-2-pentanon (4MMP) |
|
pušpan, žuka |
0,8 ng/L |
0-120 ng/L[13] |
|
|
3-sulfanilheksan-1-ol (3-SH) |
|
pasijonka, grenivka |
60 ng/L |
150-3500ng/L[14] |
||
|
|
|
|
|
|
||
|
3-sulfanilheksil acetat (3SHA) |
|
pasijonka, pušpan |
4ng/L |
0-500ng/L[15] |
||
|
Terpeni |
linalool |
|
sivka |
25 μg/L 100 μg/L[16] |
0-105 μg/L |
|
|
geraniol |
|
cvetlične note, citrusi |
30 μg/L 130 μg/L[17] |
0-70 μg/L |
||
|
1,8-cineol (evkaliptol) |
|
mentol/meta,kafra |
3,2 μg/L[18] |
0-50 μg/L |
||
|
C13-norizoprenoidi |
β-damascenon |
|
jabolko, vrtnica, med |
0,05 µg/L
|
1-10 μg/L |
|
|
β-ionon |
|
vijolica |
90 ng/L[19] |
1-5 μg/L |
||
|
laktoni |
γ-nonalakton |
|
kokos, breskev |
30 μg/L[20] |
Up 200 μg/L [21] |
|
|
δ-dekalakton |
|
marelica, kokos, ojlno, breskev |
|
5-50 μg/L |
||
|
C6-alkoholi |
heksanol |
|
rozine, cvetje, zeleno |
8000 μg/L |
< 2mg/L |
|
|
(Z)-3-heksanol |
|
trava |
400 μg/L |
|
||
|
višji alkoholi |
izomilni alkohol |
|
slad |
40000 μg/L |
mg/L |
|
|
2-feniletanol |
|
vrtnica, lilija |
10000 μg/L |
|||
|
estri |
izoamil acetat |
|
banana |
313 μg/L |
mg/L |
|
|
fenetil acetat |
|
vrtnica |
250 μg/L |
|||
|
etilbutirat |
|
jabolko |
20 μg/L |
|||
|
etilheksanoat |
|
jabolčna lupina, sadje |
14 μg/L |
|||
|
etiloktanoat |
|
sadje, mastno |
5 μg/L |
|||
|
etil izobutirat |
|
sladko, guma |
15 μg/L |
|||
|
hlapni fenoli |
gvajakol |
|
dim, sladko, zdravila |
20 μg/L 95[23] |
10-100 μg/L[24]
|
|
|
4-vinilfenol |
|
mandljeva lupina |
180 μg/L[25] |
0-1200 μg/L[26] |
||
Viri
Allamy, L., Darriet, P., in Pons, A. (2018a). Molecular interpretation of dried-fruit aromas in Merlot and Cabernet Sauvignon musts and young wines: Impact of over-ripening. Food Chemistry, 266, 245–253. https://doi.org/10.1016/j.foodchem.2018.06.022
Allamy, L., Darriet, P., in Pons, A. (2018b). Molecular interpretation of dried-fruit aromas in Merlot and Cabernet Sauvignon musts and young wines: Impact of over-ripening. Food Chemistry, 266, 245–253. https://doi.org/10.1016/j.foodchem.2018.06.022
Amerine, M. A., in Cruess, W. V. (1960). The Technology of Wine Making, by M.A. Amerine and W.V. Cruess. Avi Publishing Company. https://books.google.si/books?id=lL8lcgAACAAJ
Antalick, G., Tempère, S., Šuklje, K., Blackman, J. W., Deloire, A., de Revel, G., in Schmidtke, L. M. (2015). Investigation and Sensory Characterization of 1,4-Cineole: A Potential Aromatic Marker of Australian Cabernet Sauvignon Wine. Journal of Agricultural and Food Chemistry, 63(41), 9103–9111. https://doi.org/10.1021/acs.jafc.5b03847
Atanasova, B., Thomas-Danguin, T., Chabanet, C., Langlois, D., Nicklaus, S., in Etievant, P. (2005). Perceptual Interactions in Odour Mixtures: Odour Quality in Binary Mixtures of Woody and Fruity Wine Odorants. Chemical Senses, 30(3), 209–217. https://doi.org/10.1093/chemse/bji016
Aznar, M., in Arroyo, T. (2007). Analysis of wine volatile profile by purge-and-trap-gas chromatography-mass spectrometry. Application to the analysis of red and white wines from different Spanish regions. Journal of Chromatography. A, 1165(1–2), 151–157. https://doi.org/10.1016/j.chroma.2007.07.031
Bindon, K., Holt, H., Williamson, P. O., Varela, C., Herderich, M., in Francis, I. L. (2014). Relationships between harvest time and wine composition in Vitis vinifera L. cv. Cabernet Sauvignon 2. Wine sensory properties and consumer preference. Food Chemistry, 154, 90–101. https://doi.org/10.1016/j.foodchem.2013.12.099
Black, C. a., Parker, M., Siebert, T. e., Capone, D. l., in Francis, I. l. (2015). Terpenoids and their role in wine flavour: Recent advances. Australian Journal of Grape and Wine Research, 21(S1), 582–600. https://doi.org/10.1111/ajgw.12186
Bubola, M., Rusjan, D., in Lukić, I. (2020). Crop level vs. leaf removal: Effects on Istrian Malvasia wine aroma and phenolic acids composition. Food Chemistry, 312, 126046. https://doi.org/10.1016/j.foodchem.2019.126046
Cameleyre, M., Lytra, G., Tempere, S., in Barbe, J.-C. (2015). Olfactory Impact of Higher Alcohols on Red Wine Fruity Ester Aroma Expression in Model Solution. Journal of Agricultural and Food Chemistry, 63(44), Article 44. https://doi.org/10.1021/acs.jafc.5b03489
Carrau, F. M., Boido, E., in Dellacassa, E. (2008). Terpenoids in Grapes and Wines: Origin and Micrometabolism during the Vinification Process. Natural Product Communications, 3(4), 1934578X0800300. https://doi.org/10.1177/1934578X0800300419
Castro-Vázquez, L., Alañón, M. E., Calvo, E., Cejudo, M. J., Díaz-Maroto, M. C., in Pérez-Coello, M. S. (2011). Volatile compounds as markers of ageing in Tempranillo red wines from La Mancha D.O. stored in oak wood barrels. Journal of Chromatography A, 1218(30), 4910–4917. https://doi.org/10.1016/j.chroma.2010.12.094
Chatonnet, P., Cutzach, I., Pons, M., in Dubourdieu, D. (1999). Monitoring Toasting Intensity of Barrels by Chromatographic Analysis of Volatile Compounds from Toasted Oak Wood. Journal of Agricultural and Food Chemistry, 47(10), 4310–4318. https://doi.org/10.1021/jf981234t
Cheynier, V., Schneider, R., Salmon, J.-M., in Fulcrand, H. (2010). 3.26—Chemistry of Wine. In H.-W. (Ben) Liu in L. Mander (Eds.), Comprehensive Natural Products II (pp. 1119–1172). Elsevier. https://doi.org/10.1016/B978-008045382-8.00088-5
Coetzee, C., in du Toit, W. J. (2012). A comprehensive review on Sauvignon blanc aroma with a focus on certain positive volatile thiols. Food Research International, 45(1), 287–298. https://doi.org/10.1016/j.foodres.2011.09.017
Cordente, A. G., Espinase Nandorfy, D., Solomon, M., Schulkin, A., Kolouchova, R., Francis, I. L., in Schmidt, S. A. (2021). Aromatic Higher Alcohols in Wine: Implication on Aroma and Palate Attributes during Chardonnay Aging. Molecules, 26(16), Article 16. https://doi.org/10.3390/molecules26164979
Dekoninck, T. M. L., Verbelen, P. J., Delvaux, F., Van Mulders, S. E., in Delvaux, F. R. (2012). The Importance of Wort Composition for Yeast Metabolism during Accelerated Brewery Fermentations1. Journal of the American Society of Brewing Chemists, 70(3), 195–204. https://doi.org/10.1094/ASBCJ-2012-0809-01
de-la-Fuente-Blanco, A., Sáenz-Navajas, M.-P., in Ferreira, V. (2016). On the effects of higher alcohols on red wine aroma. Food Chemistry, 210, 107–114. https://doi.org/10.1016/j.foodchem.2016.04.021
Díaz-Maroto, M. C., Schneider, R., in Baumes, R. (2005). Formation Pathways of Ethyl Esters of Branched Short-Chain Fatty Acids during Wine Aging. Journal of Agricultural and Food Chemistry, 53(9), 3503–3509. https://doi.org/10.1021/jf048157o
Dzialo, M. C., Park, R., Steensels, J., Lievens, B., in Verstrepen, K. J. (2017). Physiology, ecology and industrial applications of aroma formation in yeast. FEMS Microbiology Reviews, 41(Supp_1), S95–S128. https://doi.org/10.1093/femsre/fux031
Escudero, A., Campo, E., Fariña, L., Cacho, J., in Ferreira, V. (2007). Analytical Characterization of the Aroma of Five Premium Red Wines. Insights into the Role of Odor Families and the Concept of Fruitiness of Wines. Journal of Agricultural and Food Chemistry, 55(11), 4501–4510. https://doi.org/10.1021/jf0636418
Etievant, P. (1991). Volatile compounds in food and beverages. Wine, 483–546.
Falcao, L. D., Lytra, G., Darriet, P., in Barbe, J.-C. (2012). Identification of ethyl 2-hydroxy-4-methylpentanoate in red wines, a compound involved in blackberry aroma. Food Chemistry, 132(1), Article 1. https://doi.org/10.1016/j.foodchem.2011.10.061
Fariña, L., Boido, E., Carrau, F., Versini, G., in Dellacassa, E. (2005). Terpene Compounds as Possible Precursors of 1,8-Cineole in Red Grapes and Wines. Journal of Agricultural and Food Chemistry, 53(5), 1633–1636. https://doi.org/10.1021/jf040332d
Farrell, R. R., Wellinger, M., Gloess, A. N., Nichols, D. S., Breadmore, M. C., Shellie, R. A., in Yeretzian, C. (2015). Real-Time Mass Spectrometry Monitoring of Oak Wood Toasting: Elucidating Aroma Development Relevant to Oak-aged Wine Quality. Scientific Reports, 5(1), Article 1. https://doi.org/10.1038/srep17334
Fernández De Simón, B., Martínez, J., Sanz, M., Cadahía, E., Esteruelas, E., in Muñoz, A. M. (2014). Volatile compounds and sensorial characterisation of red wine aged in cherry, chestnut, false acacia, ash and oak wood barrels. Food Chemistry, 147, 346–356. https://doi.org/10.1016/j.foodchem.2013.09.158
Ferreira, V., Jarauta, I., Ortega, L., in Cacho, J. (2004). Simple strategy for the optimization of solid-phase extraction procedures through the use of solid–liquid distribution coefficients: Application to the determination of aliphatic lactones in wine. Journal of Chromatography A, 1025(2), 147–156. https://doi.org/10.1016/j.chroma.2003.10.086
Ferreira, V., López, R., in Cacho, J. F. (2000). Quantitative determination of the odorants of young red wines from different grape varieties. Journal of the Science of Food and Agriculture, 80(11), 1659–1667. https://doi.org/10.1002/1097-0010(20000901)80:11%253C1659::AID-JSFA693%253E3.0.CO;2-6
Ferreira, V., Ortín, N., Escudero, A., López, R., in Cacho, J. (2002). Chemical Characterization of the Aroma of Grenache Rosé Wines: Aroma Extract Dilution Analysis, Quantitative Determination, and Sensory Reconstitution Studies. Journal of Agricultural and Food Chemistry, 50(14), Article 14. https://doi.org/10.1021/jf0115645
Ferron, P. de, Thibon, C., Shinkaruk, S., Darriet, P., Allamy, L., in Pons, A. (2020). Aromatic Potential of Bordeaux Grape Cultivars: Identification and Assays on 4-Oxononanoic Acid, a γ-Nonalactone Precursor. Journal of Agricultural and Food Chemistry, 68(47), 13344–13352. https://doi.org/10.1021/acs.jafc.0c04171
Genovese, A., Piombino, P., Gambuti, A., in Moio, L. (2009). Simulation of retronasal aroma of white and red wine in a model mouth system. Investigating the influence of saliva on volatile compound concentrations. Food Chemistry, 114(1), 100–107. https://doi.org/10.1016/j.foodchem.2008.09.022
Goodwin, T. W. (1964). Chapter 19—The Biogenesis of Terpenes and Steroids. In S. Coffey (Ed.), Rodd’s Chemistry of Carbon Compounds (Second Edition) (pp. 54–137). Elsevier. https://doi.org/10.1016/B978-044453345-6.50248-0
Guth, H. (1997). Quantitation and Sensory Studies of Character Impact Odorants of Different White Wine Varieties. Journal of Agricultural and Food Chemistry, 45(8), 3027–3032. https://doi.org/10.1021/jf970280a
Herve, E., Price, S., in Burns, G. (2003). Eucalyptol in wines showing a “eucalyptus” aroma. Proceedings of VIIeme Symposium International d’Oenologie, Eds A. Lonvaud, G. de Revel, and P. Darriet (Parise: Tec in Doc Lavoisier), 598–600.
Hjelmeland, A. K., in Ebeler, S. E. (2015). Glycosidically Bound Volatile Aroma Compounds in Grapes and Wine: A Review. American Journal of Enology and Viticulture, 66(1), 1–11. https://doi.org/10.5344/ajev.2014.14104
Iobbi, A., Di, Y., in Tomasino, E. (2023). Revealing the sensory impact of different levels and combinations of esters and volatile thiols in Chardonnay wines. Heliyon, 9(1), e12862. https://doi.org/10.1016/j.heliyon.2023.e12862
Jordão, A. M., in Cosme, F. (2022). The Application of Wood Species in Enology: Chemical Wood Composition and Effect on Wine Quality. Applied Sciences, 12(6), Article 6. https://doi.org/10.3390/app12063179
King, E. s., Osidacz, P., Curtin, C., Bastian, S. e. p., in Francis, I. l. (2011). Assessing desirable levels of sensory properties in Sauvignon Blanc wines – consumer preferences and contribution of key aroma compounds. Australian Journal of Grape and Wine Research, 17(2), 169–180. https://doi.org/10.1111/j.1755-0238.2011.00133.x
Kong, C.-L., Ma, N., Yin, J., Zhao, H.-Y., in Tao, Y.-S. (2021). Fine tuning of medium chain fatty acids levels increases fruity ester production during alcoholic fermentation. Food Chemistry, 346(128897). https://doi.org/10.1016/j.foodchem.2020.128897
Kosseva, M. R., Joshi, V. K., in Panesar, P. S. (2016). Science and Technology of Fruit Wine Production. Academic Press.
Kotseridis, Y., Baumes, R. L., Bertrand, A., in Skouroumounis, G. K. (1999). Quantitative determination of β-ionone in red wines and grapes of Bordeaux using a stable isotope dilution assay. Journal of Chromatography A, 848(1), 317–325. https://doi.org/10.1016/S0021-9673(99)00422-7
Lambrechts, M. G., in Pretorius, I. S. (2000). Yeast and its Importance to Wine Aroma—A Review. South African Journal of Enology and Viticulture, 21(1), Article 1. https://doi.org/10.21548/21-1-3560
Lei, Y., Xie, S., Guan, X., Song, C., Zhang, Z., in Meng, J. (2018). Methoxypyrazines biosynthesis and metabolism in grape: A review. Food Chemistry, 245, 1141–1147. https://doi.org/10.1016/j.foodchem.2017.11.056
Ling, M., Bai, X., Cui, D., Shi, Y., Duan, C., in Lan, Y. (2023). An efficient methodology for modeling to predict wine aroma expression based on quantitative data of volatile compounds: A case study of oak barrel-aged red wines. Food Research International, 164, 112440. https://doi.org/10.1016/j.foodres.2022.112440
Linsenmeier, A. W., Rauhut, D., in Sponholz, W. R. (2022). Aging and flavor deterioration in wine. In Managing Wine Quality (pp. 559–594). Elsevier. https://doi.org/10.1016/B978-0-08-102065-4.00037-7
López, R., Aznar, M., Cacho, J., in Ferreira, V. (2002). Determination of minor and trace volatile compounds in wine by solid-phase extraction and gas chromatography with mass spectrometric detection. Journal of Chromatography A, 966(1–2), 167–177. https://doi.org/10.1016/S0021-9673(02)00696-9
Lytra, G., Tempere, S., Marchand, S., de Revel, G., in Barbe, J.-C. (2016). How do esters and dimethyl sulphide concentrations affect fruity aroma perception of red wine? Demonstration by dynamic sensory profile evaluation. Food Chemistry, 194, 196–200. https://doi.org/10.1016/j.foodchem.2015.07.143
Marchand, S., Almy, J., in de Revel, G. (2011). The cysteine reaction with diacetyl under wine-like conditions: Proposed mechanisms for mixed origins of 2-methylthiazole, 2-methyl-3-thiazoline, 2-methylthiazolidine, and 2,4,5-trimethyloxazole. Journal of Food Science, 76(6), C861-868. https://doi.org/10.1111/j.1750-3841.2011.02261.x
Marchand, S., de Revel, G., in Bertrand, A. (2000). Approaches to wine aroma: Release of aroma compounds from reactions between cysteine and carbonyl compounds in wine. Journal of Agricultural and Food Chemistry, 48(10), 4890–4895. https://doi.org/10.1021/jf000149u
Marín-San Román, S., Rubio-Bretón, P., Pérez-Álvarez, E. P., in Garde-Cerdán, T. (2020). Advancement in analytical techniques for the extraction of grape and wine volatile compounds. Food Research International, 137, 109712. https://doi.org/10.1016/j.foodres.2020.109712
Mateo, J. J., in Jiménez, M. (2000). Monoterpenes in grape juice and wines. Journal of Chromatography A, 881(1), 557–567. https://doi.org/10.1016/S0021-9673(99)01342-4
Mateo-Vivaracho, L., Zapata, J., Cacho, J., in Ferreira, V. (2010). Analysis, occurrence, and potential sensory significance of five polyfunctional mercaptans in white wines. Journal of Agricultural and Food Chemistry, 58(18), 10184–10194. Scopus. https://doi.org/10.1021/jf101095a
Mendes-Pinto, M. M. (2009). Carotenoid breakdown products the—Norisoprenoids—In wine aroma. Archives of Biochemistry and Biophysics, 483(2), 236–245. https://doi.org/10.1016/j.abb.2009.01.008
Miller, G. C., Pilkington, L. I., Barker, D., in Deed, R. C. (2022). Saturated Linear Aliphatic γ- and δ-Lactones in Wine: A Review. Journal of Agricultural and Food Chemistry, 70(49), 15325–15346. https://doi.org/10.1021/acs.jafc.2c04527
Montalvo, F. F., García-Alcaraz, J. L., Cámara, E. M., Jiménez-Macías, E., in Blanco-Fernández, J. (2021). Environmental impact of wine fermentation in steel and concrete tanks. Journal of Cleaner Production, 278, 123602. https://doi.org/10.1016/j.jclepro.2020.123602
Moreno-Arribas, M. V., in Polo, M. C. (Eds.). (2009). Wine Chemistry and Biochemistry. Springer New York. https://doi.org/10.1007/978-0-387-74118-5
Mozzon, M., Savini, S., Boselli, E., in Thorngate, J. H. (2016). The herbaceous character of wines. Italian Journal of Food Science, 28(2), 190–207. https://doi.org/10.14674/1120-1770/ijfs.v304
Muñoz, D., Peinado, R. A., Medina, M., in Moreno, J. (2006). Higher alcohols concentration and its relation with the biological aging evolution. European Food Research and Technology, 222(5–6), 629–635. https://doi.org/10.1007/s00217-005-0161-4
Murat, M.-L., Tominaga, T., in Dubourdieu, D. (2001). Assessing the Aromatic Potential of Cabernet Sauvignon and Merlot Musts Used to Produce Rose Wine by Assaying the Cysteinylated Precursor of 3-Mercaptohexan-1-ol. Journal of Agricultural and Food Chemistry, 49(11), 5412–5417. https://doi.org/10.1021/jf0103119
Nakamura, S., Crowell, E. a., Ough, C. s., in Totsuka, A. (1988). Quantitative Analysis of γ-Nonalactone in Wines and Its Threshold Determination. Journal of Food Science, 53(4), 1243–1244. https://doi.org/10.1111/j.1365-2621.1988.tb13578.x
Ortega-Heras, M., González-Huerta, C., Herrera, P., in González-Sanjosé, M. L. (2004). Changes in wine volatile compounds of varietal wines during ageing in wood barrels. Analytica Chimica Acta, 513(1), 341–350. https://doi.org/10.1016/j.aca.2003.10.051
Palai, G., Caruso, G., Gucci, R., in D’Onofrio, C. (2023). Water deficit before veraison is crucial in regulating berry VOCs concentration in Sangiovese grapevines. Frontiers in Plant Science, 14. https://www.frontiersin.org/journals/plant-science/articles/10.3389/fpls.2023.1117572
Pérez-Prieto, L. J., López-Roca, J. M., Martínez-Cutillas, A., Pardo Mínguez, F., in Gómez-Plaza, E. (2002). Maturing Wines in Oak Barrels. Effects of Origin, Volume, and Age of the Barrel on the Wine Volatile Composition. Journal of Agricultural and Food Chemistry, 50(11), 3272–3276. https://doi.org/10.1021/jf011505r
Perry, D. M., in Hayes, J. E. (2016). Effects of Matrix Composition on Detection Threshold Estimates for Methyl Anthranilate and 2-Aminoacetophenone. Foods, 5(2), Article 2. https://doi.org/10.3390/foods5020035
Pichler, A., Ivić, I., Mesić, J., Drenjančević, M., Kujundžić, T., Marković, T., in Kopjar, M. (2024). Aroma Profile of Merlot Red Wine Stored in Stainless-Steel Tanks and Wooden Barrels with Different Toasting Methods. Foods, 13(1), Article 1. https://doi.org/10.3390/foods13010045
Pineau, B., Barbe, J.-C., Van Leeuwen, C., in Dubourdieu, D. (2007). Which Impact for β-Damascenone on Red Wines Aroma? Journal of Agricultural and Food Chemistry, 55(10), Article 10. https://doi.org/10.1021/jf070120r
Pineau, B., Barbe, J.-C., Van Leeuwen, C., in Dubourdieu, D. (2009). Examples of Perceptive Interactions Involved in Specific “Red-” and “Black-berry” Aromas in Red Wines. Journal of Agricultural and Food Chemistry, 57(9), 3702–3708. https://doi.org/10.1021/jf803325v
Pires, E. J., Teixeira, J. A., Brányik, T., in Vicente, A. A. (2014). Yeast: The soul of beer’s aroma—a review of flavour-active esters and higher alcohols produced by the brewing yeast. Applied Microbiology and Biotechnology, 98(5), 1937–1949. https://doi.org/10.1007/s00253-013-5470-0
Poitou, X., Thibon, C., in Darriet, P. (2017). 1,8-Cineole in French Red Wines: Evidence for a Contribution Related to Its Various Origins. Journal of Agricultural and Food Chemistry, 65(2), Article 2. https://doi.org/10.1021/acs.jafc.6b03042
Pons, A., Allamy, L., Lavigne, V., Dubourdieu, D., in Darriet, P. (2017). Study of the contribution of massoia lactone to the aroma of Merlot and Cabernet Sauvignon musts and wines. Food Chemistry, 232, 229–236. https://doi.org/10.1016/j.foodchem.2017.03.151
Qian, X., Jia, F., Cai, J., Shi, Y., Duan, C., in Lan, Y. (2022). Characterization and Evolution of Volatile Compounds of Cabernet Sauvignon Wines from Two Different Clones during Oak Barrel Aging. Foods, 11(1), Article 1. https://doi.org/10.3390/foods11010074
Rapp, A., in Mandery, H. (1986). Wine aroma. Experientia, 42(8), 873–884. https://doi.org/10.1007/BF01941764
Ribereau-Gayon, P., Boidron, J. N., in Terrier, A. (1975). Aroma of Muscat grape varieties. Journal of Agricultural and Food Chemistry, 23(6), 1042–1047. https://doi.org/10.1021/jf60202a050
Ribéreau-Gayon, P., Dubourdieu, D., in Donèche, B. (2006). Handbook of enology (2nd ed). John Wiley.
Ribéreau-Gayon, P., Glories, Y., Maujean, A., in Dubourdieu, D. (2017). Traité d’oenologie—Tome 2 (6th ed., Vol. 2). Dunod. https://www.dunod.com/sciences-techniques/traite-d-oenologie-tome-2-chimie-du-vin-stabilisation-et-traitements-0
Roland, A., Schneider, R., Charrier, F., Cavelier, F., Rossignol, M., in Razungles, A. (2011). Distribution of varietal thiol precursors in the skin and the pulp of Melon B. and Sauvignon Blanc grapes. Food Chemistry, 125(1), 139–144. https://doi.org/10.1016/j.foodchem.2010.08.050
Roland, A., Schneider, R., Razungles, A., in Cavelier, F. (2011). Varietal Thiols in Wine: Discovery, Analysis and Applications. Chemical Reviews, 111(11), 7355–7376. https://doi.org/10.1021/cr100205b
Roujou De Boubée, D., Van Leeuwen, C., in Dubourdieu, D. (2000). Organoleptic Impact of 2-Methoxy-3-isobutylpyrazine on Red Bordeaux and Loire Wines. Effect of Environmental Conditions on Concentrations in Grapes during Ripening. Journal of Agricultural and Food Chemistry, 48(10), 4830–4834. https://doi.org/10.1021/jf000181o
Ruiz, J., Kiene, F., Belda, I., Fracassetti, D., Marquina, D., Navascués, E., Calderón, F., Benito, A., Rauhut, D., Santos, A., in Benito, S. (2019). Effects on varietal aromas during wine making: A review of the impact of varietal aromas on the flavor of wine. Applied Microbiology and Biotechnology, 103(18), 7425–7450. https://doi.org/10.1007/s00253-019-10008-9
Sáenz-Navajas, M.-P., González-Hernández, M., Campo, E., Fernández-Zurbano, P., in Ferreira, V. (2012). Orthonasal aroma characteristics of Spanish red wines from different price categories and their relationship to expert quality judgements: Aroma properties and quality of Spanish red wines. Australian Journal of Grape and Wine Research, 18(3), Article 3. https://doi.org/10.1111/j.1755-0238.2012.00195.x
Saerens, S. M. G., Delvaux, F., Verstrepen, K. J., Van Dijck, P., Thevelein, J. M., in Delvaux, F. R. (2008). Parameters Affecting Ethyl Ester Production by Saccharomyces cerevisiae during Fermentation. Applied and Environmental Microbiology, 74(2), 454–461. https://doi.org/10.1128/AEM.01616-07
Sala, C., Busto, O., Guasch, J., in Zamora, F. (2004). Influence of Vine Training and Sunlight Exposure on the 3-Alkyl-2-methoxypyrazines Content in Musts and Wines from the Vitis vinifera Variety Cabernet Sauvignon. Journal of Agricultural and Food Chemistry, 52(11), 3492–3497. https://doi.org/10.1021/jf049927z
Salas, J., Harwood, J., in Martínez Force, E. (2013). Lipid Metabolism in Olive: Biosynthesis of Triacylglycerols and Aroma Components. In Handbook of olive oil: Analysis and properties (pp. 97–127). https://doi.org/10.1007/978-1-4614-7777-8_4
Sarrazin, E., Dubourdieu, D., in Darriet, P. (2007). Characterization of key-aroma compounds of botrytized wines, influence of grape botrytization. Food Chemistry, 103(2), 536–545. https://doi.org/10.1016/j.foodchem.2006.08.026
Sasaki, K., Takase, H., Tanzawa, F., Kobayashi, H., Saito, H., Matsuo, H., in Takata, R. (2015). Identification of Furaneol Glucopyranoside, the Precursor of Strawberry-like Aroma, Furaneol, in Muscat Bailey A. American Journal of Enology and Viticulture, 66(1), 91–94. https://doi.org/10.5344/ajev.2014.14072
Sefton, M. A., Francis, I. L., in Williams, P. J. (1990). Volatile norisoprenoid compounds as constituents of oak woods used in wine and spirit maturation. Journal of Agricultural and Food Chemistry, 38(11), 2045–2049. https://doi.org/10.1021/jf00101a009
Siebert, T. E., Barker, A., Pearson, W., Barter, S. R., de Barros Lopes, M. A., Darriet, P., Herderich, M. J., in Francis, I. L. (2018). Volatile Compounds Related to ‘Stone Fruit’ Aroma Attributes in Viognier and Chardonnay Wines. Journal of Agricultural and Food Chemistry, 66(11), 2838–2850. https://doi.org/10.1021/acs.jafc.7b05343
Slaghenaufi, D., Vanzo, L., Luzzini, G., Arapitsas, P., Marangon, M., Curioni, A., Mattivi, F., Piombino, P., Moio, L., Versari, A., Ricci, A., Segade, S. R., Rolle, L., in Ugliano, M. (2022). Monoterpenoids and norisoprenoids in Italian red wines: This article is published in cooperation with Macrowine 2021, 23-30 June 2021. OENO One, 56(3), Article 3. https://doi.org/10.20870/oeno-one.2022.56.3.5387
Slovenski standard. SIST ISO 5492, Senzorična analiza, Slovar: Ekvivalenten ISO 5492:1992 (Version 1st edition). (1997). Urad Republike Slovenije za standardizacijo in meroslovje. https://plus.cobiss.net/cobiss/si/sl/bib/um/65856768
Spillman1, P. J., Sefton, M. A., in Gawel, R. (2004). The contribution of volatile compounds derived during oak barrel maturation to the aroma of a Chardonnay and Cabernet Sauvignon wine. Australian Journal of Grape and Wine Research, 10(3), 227–235. https://doi.org/10.1111/j.1755-0238.2004.tb00026.x
Šuklje, K., Zhang, X., Antalick, G., Clark, A. C., Deloire, A., in Schmidtke, L. M. (2016). Berry Shriveling Significantly Alters Shiraz (Vitis vinifera L.) Grape and Wine Chemical Composition. Journal of Agricultural and Food Chemistry, 64(4), 870–880. https://doi.org/10.1021/acs.jafc.5b05158
Sumby, K. M., Grbin, P. R., in Jiranek, V. (2010). Microbial modulation of aromatic esters in wine: Current knowledge and future prospects. Food Chemistry, 121(1), Article 1. https://doi.org/10.1016/j.foodchem.2009.12.004
Summerson, V., Gonzalez Viejo, C., Pang, A., Torrico, D. D., in Fuentes, S. (2021). Review of the Effects of Grapevine Smoke Exposure and Technologies to Assess Smoke Contamination and Taint in Grapes and Wine. Beverages, 7(1), Article 1. https://doi.org/10.3390/beverages7010007
Tominaga, T., Baltenweck-Guyot, R., Gachons, C. P. D., in Dubourdieu, D. (2000). Contribution of Volatile Thiols to the Aromas of White Wines Made From Several Vitis vinifera Grape Varieties. American Journal of Enology and Viticulture, 51(2), 178–181. https://doi.org/10.5344/ajev.2000.51.2.178
Wang, S., Chen, P., in Dang, H. (2019). Lactic Acid Bacteria and γ-Aminobutyric Acid and Diacetyl. In W. Chen (Ed.), Lactic Acid Bacteria: Bioengineering and Industrial Applications (pp. 1–19). Springer. https://doi.org/10.1007/978-981-13-7283-4_1
Wei, Y., Chen, Z., Zhang, X.-K., Duan, C.-Q., in Pan, Q.-H. (2021). Comparative Analysis of Glycosidic Aroma Compound Profiling in Three Vitis vinifera Varieties by Using Ultra-High-Performance Liquid Chromatography Quadrupole-Time-of-Flight Mass Spectrometry. Frontiers in Plant Science, 12. https://doi.org/10.3389/fpls.2021.694979
Xue, S.-J., Zhang, J.-R., Zhang, R.-X., Qin, Y., Yang, X.-B., Jin, G.-J., in Tao, Y.-S. (2022). Oxidation-reduction potential affects medium-chain fatty acid ethyl ester production during wine alcohol fermentation. Food Research International, 157, 111369. https://doi.org/10.1016/j.foodres.2022.111369
Yuan, F., Feng, H., in Qian, M. C. (2015). C 13 -Norisoprenoids in Grape and Wine Affected by Different Canopy Management. In S. B. Ebeler, G. Sacks, S. Vidal, in P. Winterhalter (Eds.), ACS Symposium Series (Vol. 1203, pp. 147–160). American Chemical Society. https://doi.org/10.1021/bk-2015-1203.ch010
Zhu, Y., Sun, M., Harrison, R., Jordan, B., Creasy, G., in Hofmann, R. (2022). Effects of UV-B and Water Deficit on Aroma Precursors in Grapes and Flavor Release during Wine Micro-Vinification and Consumption. Foods, 11(9), Article 9. https://doi.org/10.3390/foods11091336
- Aroma ali celokupni okus (ang. flavour): senzorični vtis živila, ko ga imamo v ustih, ki ga praviloma pojasnjuje kombiniran učinek vohalnih in okušalnih zaznav. ↵
- Ortonazalno: vonj, zaznan neposredno z nosom. ↵
- Retronazalno: vonj, ki zaznamo v ustni votlini, med žvečenjem oz. uživanjem hrane (požirek vina). ↵
- Prag zaznave: najmanjša koncentracija spojine, pri kateri lahko vsaj 50 % posameznikov zazna razliko v vonjalnem dražljaju (Perry in Hayes, 2016). ↵
- Opisni izrazi (deskriptorji) po podatkih flavornet.org, obiskano januarja 2025. ↵
- Vsi pragovi so bili določeni v vodno-etanolni raztopini (9:1), razen če je navedeno drugače (Siebert in sod., 2018). ↵
- Prag določen v vodi s sladkorjem (Ribéreau-Gayon et al., 1975; Sala in sod., 2004). ↵
- (Sala in sod., 2004) ↵
- Prag določen v vodi s sladkorjem (Ribereau-Gayon in sodl., 1975). ↵
- (Sala in sod., 2004) ↵
- Prag določen v vodi (Mateo-Vivaaracho in sod., 2010). ↵
- (Sala in sod., 2004). ↵
- (Mateo-Vivaracho in sod., 2010). ↵
- (Mateo-Vivaracho in sod., 2010). ↵
- (Mateo-Vivaracho in sod., 2010). ↵
- Prag določen v vodi s ladkorjem (Ribereau-Gayon in sod., 1975). ↵
- Prag določen v vodi s sladkorjem (Ribereau-Gayon in sod., 1975). ↵
- Prag določen v rdečem vinu (Herve in sod., 2003). ↵
- Prag določen v modelnem vinu (Kotseridis in sod., 1999). ↵
- Prag določen v raztopini vinskih ekstraktov (Nakamura in sod., 1988). ↵
- (Ferreira in sod., 2004). ↵
- (Ferreira in sod., 2004). ↵
- Prag zaznave, določen v belih vinih (Summerson in sod., 2021). ↵
- Prag zaznave, določen v belih vinih (Summerson in sod., 2021). ↵
- (López n sod., 2002). ↵
- (Ribéreau-Gayon in sod., 2017) ↵